吸附平衡是指在一定温度和压力下,气固或液固两相充分接触,最后吸附质在两相中达到动态平衡;也可以是含有一定量的吸附质的惰性流体通过吸附剂固定床层,吸附质流动相和固定相中反复分配,最后在动态下达到稳定的动态平衡。达到平衡时的吸附量常用qe (单位为kg吸附质/kg吸附剂)表示。
一、单组分气相在固体上的吸附平衡
实验表明,当流体为气相时,对于一个给定的物系(即一定的吸附剂和一定的吸附质),达到吸附平衡时,吸附量与温度及压力有关,可表示为
qe =f(T,p)
当T为常熟,qe =f(p),它表明了平衡吸附量与压力之间的关系,反映这一关系的曲线称为吸附等温线。当吸附过程为放热过程时,降低温度和升高压力有利于增加气体组分的吸附量。在生产和科研中最常用得是吸附等温线。
根据实验,吸附等温线归纳为如图13—1所示的五种类型。图中纵坐标为平衡吸附量qe ,横坐标为蒸汽组分分压p和该温度下饱和蒸汽压po的 的比值p/po 。
I类 吸附出现饱和值。这种吸附相当于在吸附剂表面上形成单分子层吸附,接近Langmuir型吸附等温线。此类情况一般吸附剂毛细孔的孔径比吸附剂分子尺寸略大(属同一数量级时发生微空填充效应)。如氧在-1830 C活性炭上的吸附。
II类 其特点是不出现饱和值,随对比压力增加,平衡吸附量急剧上升,曲线上凸。吸附质的极限值对应于物质的溶解度,属于多分子层物理吸附。如-1980 C氮在催化剂上的吸附。
III类 曲线下凹,吸附气体量随组分分压增加而上升。曲线下凹是因为单分子层内分子间互相作用,使第一层的吸附热比冷凝热小,以致吸附质教难于吸附。此中情况教少见,如溴在硅胶(790 C)上的吸附。
IV类 能形成有限的多层吸附。曲线由几段构成, 线段上凸和中间段下凹。开始吸附量随着气体中组分分压的增加迅速增大,曲线凸起,吸附剂表面形成易于移动的单分子层吸附;而后一段凸起的曲线表示由于吸附剂表面建立了类似液膜层的多层分子吸附;两线段间的突变,说明有毛细孔的凝结现象。如500 C下苯在氧化铁上得吸附。
V类 曲线一开始就下凹,吸附质较难被吸附,吸附量随气体中组分浓度增加而缓慢上升,当接近饱和压力时,曲线趋于饱和,形成多层吸附,有滞后效应。如水蒸气在1000 C木炭中得吸附。
IV类与V类有滞后效应。这主要是由于出现毛细管冷凝现象和孔容得限制。
DeVault提出:沿吸附量坐标方向上上凸的吸附等温线为“优惠”等温线吸附,可以保证痕量物质脱除;而向下凹的等温线为“非优惠“的吸附等温线,如III类。五中类型等温线,反映了吸附剂的表面性质不同,以及孔的分布和吸附质分子间的作用力不同。
二、液相在固体上的吸附平衡和吸附等温曲线
液相吸附的机理比气相吸附要复杂,出温度和吸附质浓度外,溶剂本身的吸附、吸附质得性质及吸附剂种类、离子之间的相互作用等都对吸附产生不同程度的影响。对大量有机化合物吸附性能的研究表明:(1)同族序列的有机化合物相对分子质量愈大,吸附量愈高;(2)溶解度小,疏水程度高,则易吸附;(3)一般芳香族化合物比脂肪族化合物更易吸附;(3)知链化合物比侧链化合物更易吸附。
二、吸附等温方程
用来描述等温吸附平衡的数学式,称为吸附等温方程,常用的有Langmuir等温式和Freundlich等温式。
1、Langmuir等温式
朗格谬尔在研究低压气体在金属上得吸附时,根据试验数据,结合动力学得观点,提出了朗格缪尔单分子层吸附等温式:
qe=aqmpe/(1+ape) (13-1)
式中,qm—表面上吸满单分子层吸附质得吸附量,kg(吸附质)/kg(吸附剂);
pe—吸附质得平衡分压,Pa ;
a—吸附系数。
后来发现朗格缪尔公式也常用于液相吸附,故又写成下述形式
qe=aqmye/(1+a’ye) (13-2)
式中,a’ —吸附系数;
ye—吸附质在液相中得平衡浓度,摩尔分率。
由上两式可以看出,当pe(或ye)很小时,则qe=aqmpe(或qe=a’qmye),呈亨利定律形式,即平衡吸附量与流体的平衡分压(或平衡浓度)成正比;当p 时,则qe=qm,表明在吸附质分压很大时,平衡吸附量与流体得浓度无关,此时吸附剂表面都被占满,形成单分子层。
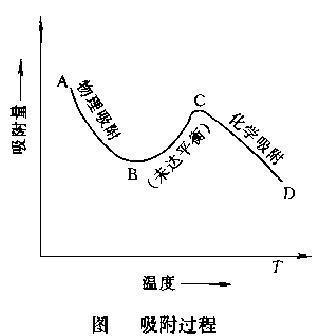
朗格缪尔关系式是一个理想得吸附公式,它代表了在均匀表面上吸附分子间彼此没有相互作用得情况下,单分子层吸附达到平衡时得规律。
2、Freundlich等温式
对于在等温情况下,吸附热随着覆盖率(即吸附量)得增加,呈对数下降得吸附平衡,Freundlich提出下列公式:
qe=kpe1/ n (13-3)
或
qe=k’ye1/ n (13-4)
式中,k,k’—Freundlich吸附系数;
n—和温度有关得常数,一般认为n=2~10时为易吸收过程;n<0.5时为难吸附过程。
Freundlich等稳式是经验公式,适用于低浓度气体或的浓度溶液未知组成物得吸附。植物油或有机质溶液的脱色也常用此式描述。值得提出的是该式尤其适用与活性炭吸附处理各种废水时的情形,此时吸附量和废水的出水浓度均能较好地满足上式。
 爱华网
爱华网