三。所谓体液免疫(humoral inmunity),即以B cells产生抗体来达到保护目的的免疫机制。负责体液免疫的细胞是B细胞。体液免疫的抗原多为相对分子质量在10,000以上的蛋白质和多糖大分子,病毒颗粒和细菌表面都带有不同的抗原,所以都能引起体液免疫。(抗原和BCR的种类都非常多,在体液免疫中B淋巴细胞的BCR
体液免疫
直接与抗原结合。一种B淋巴细胞表面只有一种BCR。一种抗原侵入体内,只有带有与这种抗原互补的BCR的B淋巴细胞才能与之结合,只有得到选择刺激的B淋巴细胞克隆才能得到扩增(克隆选择学说)。 )
简单构架:体液免疫-B淋巴细胞-浆细胞和记忆细胞(下次发挥作用)-1是浆细胞产生抗体直接中和病毒,2是浆细胞与吞噬细胞(巨噬细胞)合臂吞噬抗原。
成分要素
B细胞
B细胞产生浆细胞和记忆细胞
第一步:B细胞表面的受体分子与互补的抗原分子结合后,活化、长大,并迅速分裂产生一个有同样免疫能力的细胞群——克隆(clone)、无性繁殖系。其中一部分成为浆细胞,产生抗体;一部分发展为记忆细胞(memorycell)。
免疫细胞
第二步:需要巨噬细胞和TH细胞的参与。Mφ表面带有MHCⅡ分子,它们吞噬入侵的病原体,抗原分子经Mφ处理后表达在细胞膜上,夹在MHCⅡ分子的沟中。TH细胞表面带有不同的受体,能识别Mφ表面MHC+特异的抗原分子结合物。B细胞表面带有MHC分子,可和特异的抗原分子结合,TH细胞可刺激结合Ag的B细胞分化。这一步比第一步作用更强大。
浆细胞
浆细胞产生抗体。浆细胞一般停留在各种淋巴结。每一个浆细胞每秒钟能产生2000个抗体,它们寿命很短,经几天大量产生抗体之后就死去,而抗体则进入血液循环发挥生理作用。浆细胞产生的抗体“Y”两短臂末端高变区与抗原结合,抗体的柄端(FC)可与吞噬细胞(如巨噬细胞)上的受体结合而使抗原—抗体复合物被吞噬。
记忆细胞
记忆细胞与二次免疫反应,记忆细胞也分泌抗体,它们寿命长、对抗原十分敏感,能“记住”入侵的抗原。
当同样抗原第二次入侵时,能更快的做出反应,很快分裂产生新的浆细胞和新的记忆细胞,浆细胞再次产生抗体消灭抗原。这就是二次免疫反应。它比初次反应更快,也更强烈。
体液免疫的两个关键
产生高效而短命的浆细胞,由浆细胞分泌抗体清除抗原.
产生寿命长的记忆细胞,发生二次反应立即消灭再次入侵的同样抗原。
B细胞产生浆细胞和记忆细胞
第一步:B细胞表面的受体分子与互补的抗原分子结合后,活化、长大,并迅速分裂产生一个有同样免疫能力的细胞群——克隆(clone)、无性繁殖系。其中一部分成为浆细胞,产生
体液免疫
抗体;一部分发展为记忆( B )细胞(memorycell)。
第二步:需要巨噬细胞和TH细胞的参与。Mφ表面带有MHCⅡ分子,它们吞噬入侵的病原体,抗原分子经Mφ处理后表达在细胞膜上,夹在MHCⅡ分子的沟中。TH细胞表面带有不同的受体,能识别Mφ表面MHC+特异的抗原分子结合物。B细胞表面带有MHC分子,可和特异的抗原分子结合,TH细胞可刺激结合Ag的B细胞分化。这一步比第一步作用更强大。
浆细胞产生抗体
浆细胞一般停留在各种淋巴结。每一个浆细胞每秒钟能产生2000个抗体,它们寿命很短,经几天大量产生抗体之后就死去,而抗体则进入血液循环发挥生理作用。
浆细胞产生的抗体"Y"两短臂末端高变区与抗原结合,抗体的柄端(FC)可与吞噬细胞(如巨噬细胞)上的受体结合而使抗原—抗体复合物被吞噬。
记忆细胞与二次免疫反应
记忆细胞也分泌抗体(有部分资料说能产生抗体的只有浆细胞),它们
免疫细胞
寿命长、对抗原十分敏感,能“记住”入侵的抗原。
当同样抗原第二次入侵时,能更快的做出反应,很快分裂产生新的浆细胞和新的记忆细胞,浆细胞再次产生抗体消灭抗原。这就是二次免疫反应。它比初次反应更快,也更强烈。
体液免疫的两个关键:
(1)产生高效而短命的浆细胞,由浆细胞分泌抗体清除抗原;
(2)产生寿命长的记忆细胞,发生二次反应立即消灭再次入侵的同样抗原。
体液免疫功能的检测
临床上一个反复发作的化脓感染,常使医生想到患者是否有免疫缺陷病,一般原发免疫缺陷发病年龄很小,而继发免疫缺陷病人多在30岁以上。绝大多数免疫缺陷病人多表现为体液和细胞免疫同时受损,所以应全面检查这两方面的功能。遗憾的是,目前应用的检测方法的局限性,其结果常难以得出明确结论。
免疫球蛋白的定量检测
1.血清免疫球蛋白的测定 血清免疫球蛋白(Ig)的测定是检查体液免疫功能最常用的方法。由于目前还没有发现由IgD和IgE缺陷所致疾病,所以通常检测IgG、IgM、IgA,这三类Ig就可以代表血清Ig的水平(表20-2)。检测发现三类Ig水平均明显低下,就可考虑体液免疫缺陷。但在分析儿
免疫细胞
童Ig水平时,应注意Ig的水平随年龄而变化。体液免疫功能缺陷首先考虑患者血清Ig 水平,如果所有类别Ig水平均降低,即称为一般性联低丙种球蛋白血症。如果免疫球蛋白水平极度低下,或IgG、IgM、IgA,三类Ig总量低于2mg/ml则称为严重低丙种球蛋白血症或无丙种球蛋白血症(agammaglobulinemia)。如果只一种或两种Ig水平降低,则称为异常丙种球蛋白血症(dysgammaglobulinemia)。一般性低丙种球蛋白血症多见于继发性免疫缺陷病。无丙种球蛋白血症常见于原发免疫缺陷病。但是常有约50%IgA缺陷病人无临床症状,伴有反复感染的IgA缺陷病人常同时有IgG的缺陷。常规的定量检测血中Ig的方法是单向免疫扩散和免疫比浊法。
2.分泌型IgA(SIgA)的测定SIgA是粘膜抗感染的重要因素,但是粘膜抗感染还包括少量渗出的IgM和IgG,还有细胞免疫的作用。由SIgA缺陷病人常可检测出针对牛奶或其他食物蛋白的沉淀抗体和自身抗体,说明机体对抗原蛋白质吸收异常,同时也存在免疫调节系统的功能紊乱。一般来说血清IgA缺陷病人常伴有SIgA缺陷,反之亦然。说明在机体中血清IgA和SIgA之间有某种生物相关性。最近也有报导少数SIgA缺陷病人的血清IgA水平正常,因而分别检查血清中和分泌液中IgA水平还是有必要的。目前用免疫比浊法可较精确地测定分泌液中IgA时和IgM和IgC水平。在用单向免疫扩散和免疫比浊法定量IgA时,因抗血清是针对这两型共有的α链的,故不能区分SIgA和血清来源的IgA。而应用抗分泌小体的抗体用酶免疫分析法,可区分血清IgA和分泌型IgA,并可对SIgA进行定量。
常见抗体的测定
检测体液免疫功能的另一种方法是定量测定正常人体内的几种常见的抗体水平。常见的抗体通常是指嗜异性凝集素、抗溶血素O抗体以及麻疹病毒、脊髓灰质炎病毒的抗体。
在严重免疫缺陷病人缺乏上述抗体,常见抗体的缺损可验证或支持免疫蛋白测定的结果。然而对于比较复杂的免疫缺陷,由于这类抗体主要反映过去的免疫应答能力,此外这种初次应答能力持续期短,易于消退,所以对新近发生的继发性免疫缺陷的诊断帮助不大。
B细胞数目及功能的检测
原发性免疫缺陷和继发性免疫缺陷均可导致体液免疫功能下降。原发性体液免疫功能缺陷可能由于B细胞分化障碍,细胞内合成Ig功能紊乱或由于抑制性细胞功能过强。继发性体液免疫功能降低可能由于蛋白质大量丢失,蛋白质吸收障碍、营养不良、免疫抑制治疗的副作用,病毒感染(艾滋病)等。在诊断原发性体液免疫功能缺损中可检查B细胞的数目和功能以确定造成缺损的原因。
1.外周血B细胞数目的检测首先进行常规的外周血白细胞总数和分类计数检查,这些结果是评价病人免疫系统功能状态的基本资料。由于在全血中淋巴细胞所占比例很少,而T细胞和B细胞不能藉形态学特征分类,所以外周血B细胞数检测需先从全血分离出富含淋巴细胞的单个核细胞(peripheralblood mononuclearcell,PBM)。再依靠B细胞表面有免疫球蛋白分子或其他特征来检查B细胞。常用的方法是将待检者的PBM用FITC标记的免疫抗人Ig作直接免疫荧光染色,在荧光显微镜下显荧光的细胞为带有表面免疫球蛋白的B细胞。正常人B细胞的约占PBM的10%。
2.外周血B细胞功能的检测 分离受检者血液PBM细胞,体外培养时加入B细胞刺激物如RWM(美洲商陆刺激素)或SAC(金黄色莆萄球菌来源的刺激物)后由B细胞变成Ig分泌细胞的数量。体液免疫功能缺损患者,其PBM对PWM和SACA刺激的反应降低,产生Ig分泌细胞数正常人显著减少。在进一步检查这种免疫缺损的原因,则应检查是由B细胞或TH细胞缺损所致,还是由于TS细胞数量或活性增强引起的。
抗体形成细胞计数:检查人类Ig分泌细胞是用反向溶血空斑检测(reversedhemolytic plaqueassay)法。将待检人的PBM、用SPA包被的SRBC(SPA-SRBC)、兔抗人Ig抗体、补体四种成分混合,灌入用两张玻片做成的小室,密封好,放入温箱培养1-3小时,,在此期间,作为抗人Ig抗体的免疫IgG的FC段可与SRBC表面SPA结合,当Ig分细胞分泌出游离的Ig分子时,这些人Ig分子与SRBC表面的抗人Ig抗体结合形成免疫复合物,即可活化补体,使SPA-SRBC溶解,因此在Ig分泌细胞周围形成一个圆形的溶血区,称为溶血空斑,每一个溶血的空斑就代表一个Ig分泌细胞。
检查小鼠Ig分泌细胞应用的溶血空斑试验比较简单,即SRBC免疫注射小鼠,4天后取脾制成单个细胞悬液,加入一定量SRBC(靶细胞)混合,在补体参加下,产生抗体的细胞分泌出的Ig与SRBC(抗原)结合在补体作用下,溶血,表现肉眼可见的溶血空斑。计数空斑数代表分泌抗体的细胞数。
循环过程
体液免疫是一个相当复杂的连续过程,大体上可以分为三个阶段。
感应阶段
抗原进入机体后,除少数可以直接作用于淋巴细胞外,大多数抗原都要经过吞噬细胞的摄取和处理,经过处理的抗原,可将其内部隐蔽的抗原决定簇暴露出来。然后,吞噬细胞将抗原呈递给T细胞,刺激T细胞产生淋巴因子。少数抗原可以直接刺激B细胞。
反应阶段
B细胞接受抗原刺激后,开始进行一系列的增殖分化,形成效应B细胞。在这个过程中,有一小部分B细胞成为记忆细胞,该细胞可以在体内抗原消失数月乃至数十年以后,仍保持对抗原的记忆。当同一种抗原再次进入机体时,记忆细胞就会迅速增殖、分化,形成大量的效应B细胞,继而产生更强的特异性免疫反应,及时将抗原清除。
效应阶段
在这一阶段,抗原成为被作用的对象,效应B细胞产生的抗体可以与相应的抗原特异性结合,发挥免疫效应。例如,抗体与入侵的病菌结合,可以抑制病菌的繁殖或是对宿主细胞的黏附,从而防止感染和疾病的发生;抗体与病毒结合后,可以使病毒失去侵染和破坏宿主细胞的能力。在多数情况下,抗原抗体结合后会发生进一步的变化,如形成沉淀或细胞集团,进而被吞噬细胞吞噬消化,等等。
免疫异同
体液免疫
指B细胞在T细胞辅助下,接受抗原刺激后形成效应B细胞和记忆细胞。效应B细胞产生的具有专一性的抗体与相应抗原特异性结合后完成的免役反应。体液免疫的关键过程是产生高效而短命的效应B细胞,由效应B细胞分泌抗体清除抗原。产生寿命长的记忆细胞,在血液和淋巴中循环,随时“监察”,如有同样抗原再度入侵,立即发生免疫反应以消灭之(二次反应)。
免疫功能
而且还相互配合共同发挥免疫效应。病毒感染过程中,往往是先通过体液免疫来阻止病毒在机体内传播,若病毒已经侵染到寄主细胞中,就要通过细胞免疫.这是效应T细胞与靶细胞结合,使靶细胞通透性改变,渗透压发生变化,最终导致靶细胞破裂死亡。
胞内寄生物
体液免疫先起作用,阻止寄生物的散播感染;当寄生物进入细胞后细胞免疫将抗原释放;再由体液免疫最后清楚。若细胞免疫不存在时,体液免疫也将大部分丧失。
机体关系
机体内各系统可抽象地以集合概念表明,则神经,免疫和内分泌三系统间的关系可以图10-1中的集合群表示。其中三个集合两两重叠处可分别代表神经(N)与免疫(I),免疫(I)与内分泌(E)及神经(N)与内分泌(E)间的共同范畴,而三重叠部应视为神经、免疫和内分泌的共同内容(NIE)。集合间各有种组合方式可罗列如表10-1和图10-2。
图10-1神经(N)、免疫(I)和内分泌(E)系统的关系
体液免疫
机体关系
图10-2N、I、E间作用方式
由表10-1可见,神经免疫内分泌学(NIE)与神经内分泌学(NE)、神经免疫学(NI)和免疫内分泌学(IE)相比,涉及更为复杂的系统间影响和作用。内内涵广泛,并以NE、NI和IE间的联系为基础。系统间作用方式,既有直接和间接之分,亦要同时和先后之别,系统间交互作用的性质可为增强、减弱、修饰、允许或协同,借变频、变时和变力等方式体现。系统间作用的属性,可有生理和病理性之分,是质和量的互变过程。上述关系图示为二维描述,实际应为立体过程,结合时间变量,则三大系统间的交互影响即为四维图象,这难以直观图示。
鉴于目前描述神经,免疫和内分泌系统间关系的术语较多且易混淆,缺乏统一性,故应确定术语的范畴及相互关联系,以决定相应学科内容及领域。
作用机制
当抗原(病菌或病毒)第一次感染人体时,会被先天免疫的细胞所吞噬、清除,而其中一部分细胞特称APC——在刺激B细胞方面主要为树状细胞(dendriticcells),APC抗空呈现细胞(antigen.presenting cell),它们除了能吞噬、分解抗原,还能将分解后的碎片(一小段peptides)呈现(present)给Bcell,使之活化、分裂,并经clonoalselection(细胞细选择、株落选择)节选出对抗原最具亲和力的抗体,(此时为lgm),抗体的变异区(variableregion)能与抗原产生专一性的结合,阻止它感染正常细胞,并用另一端的FCportion与巨噬细胞结合,使巨噬细胞吞噬抗原,达到消菌的目的。
活化的B细胞在过一段时日(通常大于四周)后会把分泌的抗体由lgm转变为lgG。lgG在人体的寿命远较lgm长,约六个月。受过第一次刺激的B细胞在四周后变为记忆B细胞(menorycells),除了分泌lgG外,它还能在第二次感染时以更快的时间产生更多的抗体,同时,menory Bcell在人体特定抗原的感染而言是具有终身的保护作用的。这也是是打疫苗能保护一个人免疫受特定病菌感染的原因。
相关术语
在现代内分泌学的理论体系中,“内分泌”概念应包括内分泌、神经内分泌、旁分泌和自分泌等方式;而激素的内涵亦大为增加,诸如局部激素、循环激素、神经激素等,而许多免疫因子如淋巴因子和单核因子等均符合激素的标准;严格地讲,神经系统和免疫系统既与内分泌系统有种种区别,又有诸多共性,这也是系统间相互影响的基础。表10-1N、I、E间的作用和联系方式及相应学科划分。
细胞免疫和体液免疫是借助于血液循环、淋巴循环或组织液而进行和实现的生理过程,而神经内分泌调控也最终由循环血液或组织液完成,故在此交汇路途上难免发生交叉性影响和作用。所以神经内分泌或免疫内分泌联系在活体内必将受到免疫或神经源性因素的影响。已研究的神经免疫学领域和内容,绝大多数发现有内分泌因素或成份的参与。精神和心理活动以及行为的共同基础是中枢神经系统的高级功能活动,由此可把精神神经免疫学(psychoneuroimmunology)及行为神经免疫心理学(behaviouralneuroimmunololgy)划入神经免疫内分泌学(neuroimmunoendocrinology),作为其重要的分支学科。
神经免疫内分泌学可直接引用神经科学、免疫学和内分泌学的相关概念和理论,其研究方法应是跨学科的,研究工作应采用多重指标,全面观察,对相关临床问题的考察,更应从多方面入手,分清主次矛盾,并应考虑与其它系统的联系和影响,以期在不同水平上全面而完整地反映机体的真实生理过程。
细胞免疫过程:
简单构架:T细胞-1是致敏T细胞(效应T细胞)产生直接杀伤,2是致敏T细胞产生细胞因子(白细胞产生的白介素 干扰素 肿瘤坏死因子集落刺激因子 趋化性细胞因子 生长因子)间接杀灭病原。
细胞免疫:广义指经特异性细胞(如细胞毒T淋巴细胞)和非特异性细胞(如巨噬细胞、自然杀伤细胞)活性增强的免疫反应;狭义指T细胞介导的免疫。
细胞免疫大战细胞免疫(cellular immunity)T细胞受到抗原刺激后,增殖、分化、转化为致敏T细胞(也叫效应T细胞),当相同抗原再次进入机体的细胞中时,致敏T细胞(效应T细胞)对抗原的直接杀伤作用及致敏T细胞所释放的细胞因子的协同杀伤作用,统称为细胞免疫。
简介 同体液免疫一样,细胞免疫的产生也分为感应、反应和效应三个阶段。其作用机制包括两个方面:(1)致敏T细胞的直接杀伤作用。当致敏T细胞与带有相应抗原的靶细胞再次接触时,两者发生特异性结合,产生刺激作用,使靶细胞膜通透性发生改变,引起靶细胞内渗透压改变,靶细胞肿胀、溶解以致死亡。致敏T细胞在杀伤靶细胞过程中,本身未受伤害,可重新攻击其他靶细胞。参与这种作用的致敏T细胞,称为杀伤T细胞。(2)通过淋巴因子相互配合、协同杀伤靶细胞。如皮肤反应因子可使血管通透性增高,使吞噬细胞易于从血管内游出;巨噬细胞趋化因子可招引相应的免疫细胞向抗原所在部位集中,以利于对抗原进行吞噬、杀伤、清除等。由于各种淋巴因子的协同作用,扩大了免疫效果,达到清除抗原异物的目的。 在抗感染免疫中,细胞免疫主要参与对胞内寄生的病原微生物的免疫应答及对肿瘤细胞的免疫应答,参与迟发型变态反应和自身免疫病的形成,参与移植排斥反应及对体液免疫的调节。也可以说,在抗感染免疫中,细胞免疫既是抗感染免疫的主要力量,参与免疫防护;又是导致免疫病理的重要 因素。 T细胞是细胞免疫的主要细胞。其免疫源一般为:寄生原生动物、真菌、外来的细胞团块(eg:移植器官或被病毒感染的自身细胞)。细胞免疫也有记忆功能。(一).细胞免疫的机制和过程
几乎所有的细胞表面都有MHC-I,CD8+T细胞能识别细胞表面的MHCI+抗原复合物,识别后进行攻击。 根据功能不同T细胞可分为三类,其表面均有相应的受体,具有抗原特异性:细胞毒性T细胞免疫示意图
细胞(Cytotoxic T cells,Tc)、辅助性T细胞(helper T cells,TH)、抑制性T细胞(suppressor TCells, Ts)。Tc细胞
作用是消灭外来病原。 病毒感染细胞后,细胞表面呈现病毒表达的抗原,并结合到细胞表面的MHC-I类分子的沟中,形成MHC-抗原结合物。被Tc细胞接触、识别后,Tc分泌穿孔素(perforin),使靶细胞溶解而死,病毒进入体液,被抗体消灭。癌变细胞也是Tc攻击目标,免疫功能低下的人群容易患癌症。TH细胞
—CD4 receptor 又称辅助性T细胞,对各种免疫细胞,Tc、Ts、B都有辅助作用,对于免疫具有重要作用。 TH的受体能识别与MHC-II结合的外来抗原。MHC-II类分子存在于巨噬细胞和B细胞表面。巨噬细胞吞噬入侵的细菌等微生物,在细胞内消化、降解,抗原分子与MHC-II类结合呈现在细胞表面,将抗原传递给具有相同MHC-II类分子的TH,同时,Mφ分泌白介素-1,刺激TH,促使其分泌白介素-2,它促进TH,形成正反馈,刺激T淋巴细胞分化出Tc,刺激B细胞分化出浆细胞和记忆细胞。Ts细胞
—CD8 receptor 抑制性T细胞,只有在TH的刺激下才发生作用。在外来的抗原消灭殆尽时,发挥作用而结束“战斗”。(二)细胞免疫的全过程:
在细胞免疫中蛋白类抗原由抗原提呈细胞(APC)处理成多肽,它与MHC结合并移至APC表面,产生活化TCR信号;而抗原与T淋巴细胞表面的有关受体结合就产生第二膜信号,协同刺激信号。在双信号刺激下,T淋巴细胞才能被激活就是Bretcher-Cohn双信号模式。T淋巴细胞被激活后转化为淋巴母细胞,并迅速增殖、分化,其中一部分在中途停下不再分化,成为记忆细胞;另一些细胞则成为致敏的淋巴细胞,其中Tc有杀伤力,使外源细胞破裂而死亡。TH细胞分泌白介素等细胞因子使Tc、Mφ以及各种有吞噬能力的白细胞集中于外来细胞周围,将外来细胞彻底消灭。 在这一反应即将结束时,Ts开始发挥作用,抑制其他淋巴细胞的作用,终止免疫反应。 记忆细胞不直接执行效应功能,留待再次遇到相同抗原刺激时,它将更迅速、更强烈地增殖分化为效应细胞,有少数记忆细胞再次分裂为记忆细胞,持久地执行特异性免疫功能。(三)细胞免疫与器官移植
器官移植在同卵双胞胎之间进行较易成功,这是因为两者的基因组是一样的,细胞表面的MHC分子也是一样的,2个个体都不排斥对方的器官。 激素、放射线照射、药物(6-巯基嘌呤)等可以抑制受体的免疫功能,增加移植手术的成功率。但它同时增加了感染疾病的可能性。虽然环孢素(cyclosporin)选择性抑制T细胞的功能,但也会影响免疫系统的其他功能。 临床器官移植还存在外来器官排斥受体的问题:例如骨髓移植,当供着骨髓植入受者后,外来骨髓的淋巴细胞对受体的各组织(抗原)进行攻击,其后果可致受者死亡。细胞免疫什么时候开始发挥作用
T细胞受到抗原刺激后,分化、增殖、转化为致敏T细胞,当相同抗原再次进入机体,致敏T细胞对抗原的直接杀伤作用及致敏T细胞所释放的淋巴因子的协同杀伤作用,统称为细胞免疫。同体液免疫一样,细胞免疫的产生也分为感应、反应和效应三个阶段。其作用机制包括两个方面:(1)致敏T细胞的直接杀伤作用。当致敏T细胞与带有相应抗原的靶细胞再次接触时,两者发生特异性结合,产生刺激作用,使靶细胞膜通透性发生改变,引起靶细胞内渗透压改变,靶细胞肿胀、溶解以致死亡。致敏T细胞在杀伤靶细胞过程中,本身未受伤害,可重新攻击其他靶细胞。参与这种作用的致敏T细胞,称为杀伤T细胞。(2)通过淋巴因子相互配合、协同杀伤靶细胞。如皮肤反应因子可使血管通透性增高,使吞噬细胞易于从血管内游出;巨噬细胞趋化因子可招引相应的免疫细胞向抗原所在部位集中,以利于对抗原进行吞噬、杀伤、清除等。由于各种淋巴因子的协同作用,扩大了免疫效果,达到清除抗原异物的目的。 在抗感染免疫中,细胞免疫主要参与对胞内寄生的病原微生物的免疫应答及对肿瘤细胞的免疫应答,参与迟发型变态反应和自身免疫病的形成,参与移植排斥反应及对体液免疫的调节。也可以说,在抗感染免疫中,细胞免疫既是抗感染免疫的主要力量,参与免疫防护;又是导致免疫病理的重要因素。 T细胞是细胞免疫的主要细胞。其免疫源一般为:寄生原生动物、真菌、外来的细胞团块(eg:移植器官或被病毒感染的自身细胞)。细胞免疫也有记忆功能。免疫细胞化学术
免疫细胞化学(immunocytochemistry) 是将免疫学基本原理与细胞化学技术相结合所建立起来的新技术,根据抗原与抗体特异性结合的点,免疫荧光技术示意图
检测细胞内某种多肽、蛋白质及膜表面抗原和受体等大分子物质的存在与分布。肽类与蛋白质种类繁多,均具有抗原性,当将人或动物的某种肽或蛋白质作为抗原注入另一种动物体内,则产生与该抗原相应的特异性抗体(免疫球蛋白);将抗体从血清中提出后,结合上某种标记物,即成为标记抗体。用标记抗体与组织切片标本孵育,抗体则与细胞中相应抗原发生特异性结合,结合部位被标记物显示,则在显微镜下观察到该肽或蛋白质的分布。用荧光素(常用异硫氰酸)标记抗体,并于荧光显微镜下观察,称免疫荧光术。如抗体与辣根过氧化物酶(horseradish peroxidase, HRP)等结合,进行酶显示后,可在光镜或电镜观察,用于电镜者则称为免疫电镜术(immunoelectronmicroscopy)此外,以铁蛋 标记抗体白标记抗体,称铁蛋白标记法,也能用于电镜下观察。标记抗体与抗原结合方式直接法
用标记抗体与抗体中的相应抗原直接结合,操作方法简便,特异性高,但敏感性较差,此法可用于检定未知抗原;间接法
先用未标记的具有特异性的第一抗体与样品中的相应抗原结合,然后再以标记的第二抗体与特异性的第一抗体结合;第二抗体是用第一抗体作为抗原注入另一动物体内诱导产生的抗体,然后再结合以标记物。通过这样的放大作用,使抗原分子上的标记物大大增多,故间接法较直接法的敏感性大为增高,约高5~10倍,故应用更为广泛。间接法中较常用的,如过氧化物酶-抗过氧化物酶复合物法(peroxidaseanti-peroxidasecomplexmethod, 标记方法PAP法),该法除需一抗和二抗外,还需要制备HRP标记的抗酶抗体,即以HRP作为抗原免疫动物,制成抗HRP抗体,再以HRP对标记该抗体,制成稳定的环形PAP复合物。标本先后经一抗、二抗和PAP复合物处理后再以DAB显色抗原存在部位可见棕黄色产物。 近10年来,免疫细胞学技术有了很大进展,各种新方法相继建立。单克隆抗体 (monoclonalantibody)制备技术极大地提高抗体的特异性与免疫组化染色的精确性。继PAP法之后由于生物素-亲合素等试剂的应用,为检测微量抗原、受体、抗体提供了更精确的技术。目前常用的生物素-亲合方法有:标记亲合素-生物素法(labelledavidin-biotin method LAB法)、桥连亲合素-生物素法(bridged avidin-biotin method,BAB法)及亲素-生物素-过氧化物酶复合物法(avidin-biotin-peroxidase complexmethod,ABC法);现市上有配制成的ABC药盒供应,使用简便,是目前广泛应用的一种方法。 鸡免疫器官:免疫系统是脊椎动物和人类的防御系统;与神经系统、内分泌系统、呼吸系统等一样,是机体的一个重要的系统。免疫系统是在系统发生过程中,长期适应外界环境而进化形成的,巧妙而复杂。免疫系统包括免疫器官、无被膜淋巴组织、免疫细胞以及免疫分子等。免疫器官、免疫细胞和免疫分子相互关联、相互作用,共同协调,完成机体免疫功能。 免疫系统的组成 |
第一节免疫器官
免疫器官是指实现免疫功能的器官和组织,因为这些器官的主要成分是淋巴组织,故也称淋巴器官。
免疫器官(immunologicorgan),按功能不同分为两类:
(1)中枢淋巴器官:由骨髓及胸腺组成,主要是淋巴细胞的发生、分化、成熟的场所,并具有调控免疫应答的功能;
(2)周围淋巴器官:由淋巴结、脾脏、扁桃腺以及黏膜相关淋巴组织等组成,是成熟免疫细胞定居以及执行应答功能的部位。
一、中枢免疫器官
1、骨髓(Bone marrow)
骨髓是机体重要的造血器官,是产生各类细胞的源泉。动物出生后一切血细胞均来自骨髓,同时骨髓也是各种免疫细胞发生和分化的场所。骨髓中的多能干细胞(又称造血母细胞)首先分化成髓样干细胞和淋巴干细胞,髓样干细胞进一步分化成红细胞系、单核细胞系、粒细胞系和巨核细胞系等;后者则发育成各种淋巴细胞的前体细胞,如一部分淋巴干细胞分化为T细胞的前体细胞,随血流进入胸腺后,被诱导并分化为成熟的淋巴细胞称为胸腺依赖性淋巴细胞,简称T细胞,参与细胞免疫。一部分淋巴干细胞分化为B细胞的前体细胞。在鸟类,这些前体细胞随血流进入腔上囊发育为成熟的B细胞,又称囊依赖性淋巴细胞,参与体液免疫。在哺乳动物,这些前体细胞则在骨髓内进一步分化发育为成熟的B细胞,因此骨髓也是形成抗体的重要部位。
2、胸腺(Thymus)
是胚胎期发生最早的淋巴组织,出生后逐渐长大,青春期后开始逐渐缩小,以后缓慢退化,逐渐被脂肪组织代潜,但仍残留一定的功能。
胸腺的功能是培育大量T细胞亚群,所以说胸腺是T细胞分化成熟的场所。T细胞的分化成熟是在胸腺上皮细胞产生的数种胸腺肽类激毒诱导下完成的。
另外,来自骨髓的前T细胞,在胸腺中生长过程中,绝大多数细胞死亡,只有少于5%的前T细胞与化成熟为有功能的T细胞亚群,其意义是消除对自体成分起反应的“禁忌细胞克隆”及缺气免疫能力细胞克隆,以防引起自身免疫反应或造成免疫力不足的缺陷。
成熟的T细胞亚群随血流迁移至外国免疫器官定居。
3、腔上囊
是位于禽类泄殖腔上方的一个盲囊状结构,故称腔上囊;在300年前意大利的解剖学家H.Fabricius曾对它进行研究,故又称法氏囊(Bursaof Fabricius)。
雏鸡一日龄时,囊重50~80mg,3~4月龄时体积最大,达3~4g,性成熟后逐渐退化萎缩。鸭、鹅的腔上囊退化较慢,7日龄开始退化,12个月后几乎完全消化。
腔上囊是诱导分化B细胞成熟的场所。许多试验证明,腔上囊的造血干细胞不是产于囊内,而是源于囊外器官。Moore和Owen主张干细胞来源于卵黄囊,经血循环迁移到腔上囊。来自卵黄囊的干细胞在囊微环境的作用下,被诱导分化为囊依赖性淋巴细胞,简称B细胞,此细胞从囊内不断排入血流,分布于脾脏、淋巴结的特定部位定居,并继续增殖。B细胞受到抗原刺激后可转化为浆细胞产生抗体,发挥特异性体液免疫作用。
哺乳动物没有腔上囊,其类同器官曾认为肠道的Peyer's结(集合淋巴洁)相当于腔上囊的淋巴组织,肠淋巴滤泡、阑尾和扁桃体也为腔上囊类似组织,但它们又不符合一级淋巴器官的标准。现在普遍认为哺乳动物并不存在独立的囊类似结构,相当于腔上囊的功能由骨髓兼管,B细胞在骨髓发育成熟。
二、外周免疫器官
外周免疫器官不但是成熟的T细胞和B细胞定居的场所,而且是这些细胞受抗原刺激后发生免疫应答的部位。
1、淋巴结(Lymph node)
淋巴结是体内重要的防御关口,沿着淋巴管的路径分布。是淋巴细胞定居和增殖的场所,免疫应答的发生基地,淋巴液过滤的部位,淋巴细胞再循环的重要组成环节
(1)构造:皮质和髓质
(2)具有的功能
①过滤; ②免疫反应; ③淋巴再循环; ④清除淋巴异物
(3)注 意:
①猪的淋巴结结构与其他动物不同,其组织图象呈相反形式
②鸡没有淋巴结,淋巴组织广泛分布于体内:
有的弥散性分布;有的呈小结状;有的为淋巴孤结;有的为淋巴集结(如盲肠扁桃体、食管扁桃体)
③水禽只有颈胸和腰两对淋巴结。(鸭、鹅)
2、脾(Spleen)
是机体最大的免疫器官,含大量B,少量T,除具有与淋巴结相似的功能外,还有造血和清除自身衰老的血细胞和免疫复合物的功能。
3、黏膜相关淋巴组织
黏膜相关淋巴组织是构成机体抵抗病原入侵的第一道免疫屏障,局部黏膜的免疫状况决定着人畜机体是否被感染的首要因素。
分布:呼吸道、胃肠道、泌尿生殖道以及外分泌腺。
黏膜免疫系统在胎儿期就已开始发育,但在出生时还未发育完全。随着年龄的增长,受骨髓和胸腺的影响以及在抗原的刺激下逐步完善。
(1)肠黏膜相关淋巴样组织(Gut-associatedLymphoid Tissue,GALT)
(2)支气管黏膜相关淋巴样组织(Bronchus-associatedLymphoid Tissue,BALT)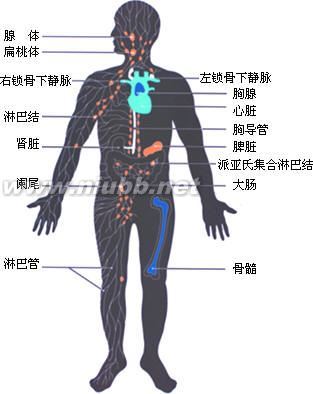
(3)眼结膜相关淋巴样组织(Conjunctiva-assoiatedLymphoid Tissue, CALT)
(4)鼻相关淋巴样组织(Nose-associatedLymphoid Tissue,NALT)。
4、扁桃体(Tonsils)以及哈德尔氏腺(Harder's gland)
扁桃体位于鼻咽部以及盲肠的黏膜层下。 哈德尔氏腺是禽类眼窝的内分泌腺。 | 它们都是重要的外周淋巴组织。 |
第二节免疫细胞
在人和动物的血液中,存在形态不同、功能各异的多种血细胞,它们是:红细胞、粒细胞、单核细胞、淋巴细胞及血小板。其生命各不相同,但起源于共同的祖先细胞,即造血干细胞。
粒细胞、单核细胞、淋巴细胞,统称为白细胞。20%的白细胞是淋巴细胞
免疫细胞(immunpcyte)是所有参与免疫反应的细胞及其前身细胞的统称。包括造血干细胞、淋巴细胞、单核巨噬细胞、树突状细胞和粒细胞等。免疫细胞可分为以下几大类:(1)淋巴细胞:包括T细胞,B细胞,NK细胞等;(2)辅佐细胞,包括巨噬细胞,树突状细胞(既抗原提呈细胞)等;(3)其它细胞,包括肥大细胞,有粒白细胞等。
免疫活性细胞是指机体受到抗原物质刺激后能分化增殖、发生特异性免疫应答、产生抗体或淋巴因子的免疫细胞。主要是:T细胞和B细胞。
一、淋巴细胞的来源
淋巴细胞是构成机体免疫系统的主要细胞群体,人体大约有1012个淋巴细胞;淋巴细胞来源于造血干细胞。
二、淋巴细胞的形态
在形态上有大中小3种类型。
1、T细胞和B细胞
均为球形,较小,5~7μm,胞浆少,核浆比大;核呈弯月形,细胞膜有不同程度的突起;T细胞绒毛较少;B细胞绒毛较多——毛球状。
2、免疫母细胞
淋巴细胞受抗原或植物血凝素等刺激后,细胞增大至原来的3~4倍,核浆比小。可进一步分化、增殖。
(1)淋巴母细胞→分化、增殖→效应淋巴细胞; (2)网状细胞样母细胞→分化、增殖→浆母细胞。
3、浆母细胞为浆细胞的前体细胞,球形,7~15μm,核浆比小,高尔基体发达。 4、浆细胞球形或椭球形,大小不等,7~15μm,胞浆丰富,嗜碱性,车轮状核,高尔基体发达。 三、免疫细胞的膜分子 |
免疫应答过程依赖于免疫系统中细胞间的相互作用,包括:细胞间直接接触、通过释放细胞因子或其它介质间接的作用。
免疫细胞间或介质与细胞间相互识别的物质基础是免疫细胞膜分子,包括细胞表面的多种抗原,受体和其它分子,细胞膜分子通常也称为细胞表面标记(cellsurface marker)。
淋巴细胞的表面标记是指存在于细胞表面的多种膜分子,是淋巴细胞识别抗原、与其他免疫细胞相互作用以及接受微环境刺激的分子基础,也是鉴别和分离淋巴细胞的重要依据。
免疫细胞分子的种类相当繁多,主要有: 1、白细胞分化抗原 2、T细胞抗原识别受体(TCR) 3、B细胞抗原识别受体(BCR) 4、抗体的Fc段受体(FcR) 5、主要组织相容性抗原(MHC类抗原) 6、粘附分子 7、促分裂素受体 8、细胞因子受体 9、其它受体和分子 等等 |
四、T淋巴细胞
T细胞即T淋巴细胞,T淋巴细胞是胸腺依赖性淋巴细胞的简称。定位于周围淋巴结的副皮质区及脾脏白髓部分,并可经血液、组织、淋巴不断释放到外周血循环中。T细胞受到抗原刺激后,将进一步活化、增殖、分化,发挥特异性细胞免疫功能。
1、T细胞表面受体
(1)T细胞抗原识别受体(TCR)
TCR是T细胞识别蛋白质抗原的特异性受体,不同的T细胞克隆其抗原识别受体的分子结构也是不相同的。大多数成熟T细胞(约占95%)的TCR分子,是由α和β二条异二聚体肽链组成的TCRαβ分子。二条肽链都由膜外区、穿膜区及胞浆区组成。在通常情况下,异种蛋白抗原分子必须与细胞表面的自身MHC分子结合才能被TCR识别。所以TCR只能识别细胞膜上MHC分子与抗原分子结合的复合物,而不能识别可溶性抗原分子,这是与B细胞识别抗原的主要不同特性。
另一种TCR是由γ和δ链组成的TCRγδ分子,它是由γ和δ基因编码的分子。它们可能是具有原始受体的第一防线的防御细胞,与清除表皮及上皮细胞内遗物有关。它们可识别高度保守的抗原,如结核杆菌、肠毒素和热休克蛋白等抗原,在人和小鼠均表明它们可识别MHC或MHC样分子。
(2)CD3分子 此分子可表达于所有成熟T细胞表面,它是由五条肽链非共价结合组成的复合分子,分别称为γ、δ、ε、ζ、和η链。五条肽链均由胞外区、穿膜区和胞浆区组成。γ、δ和ε为单体,ζ和η二条链其胞外区可由二硫链连接组成同二聚体ζ(约占90%)和异二聚体ζη分子(约占10%)。CD3分子可与TCR分子以非共价结合形成TCR-CD3复合受体分子,是T细胞识别抗原的主要识别单位,其中TCR是识别异种抗原和自身MHC分子多态性决定簇的受体,而CD3分子并不参于抗原识别,它具有稳定TCR结构和传递活化信号的作用。 (3)CD4和CD8分子 这二种分子可同时表达于胸腺内早期胸腺细胞,称为双阳性胸腺T细胞(CD4+、CD8+、DP)。 |
而在成熟T细胞这二种分于是互相排斥的,只能表达一种分子,故可将成熟T细胞分为二类,即CD4+T细胞和CD8+T细胞。
这二种分子可同时表达于胸腺内早期胸腺细胞,称为双阳性胸腺T细胞(CD4+、CD8+、DP)。在外周淋巴组织中CD4+T细胞约古65%,CD8+T细胞约占35%。这二种分子同属于Ig超家族,都不具有多样性,其分子结构都由胞外区、穿膜区及胞内区组成。CD4子为55kD的单体,CD8分子为34kD多肽组成的双体分子。这二种分子与抗原识别无关,但可与带有MHC分子的细胞结合,它们是细胞与细胞间相互作用的粘附分子。CD4分子是MHC-Ⅱ类分子的受体,它可与MHC-Ⅱ分子的非多态区结合。CD8分子可与MHC-I类分子的非多态区结合。因此这二种分子具有增强TCR与抗原递呈细胞或靶细胞的亲和性,并有助于激活信号的传递。
(4)CD28分子
这种分子可表达于全部CD4+T细胞及50%CD8+T细胞。它是80~90kD的由二硫键连接的同源二聚体分子,属于Ig基因超家族。研究证明T细胞活化需要双信号,即由TCR-CD3复合分子提供起始信号或第1信号,还必须有协同刺激信号(Costimulatorysignal)或第2信号才能使T细胞活化。在T细胞膜上已发现有多种分子与协同刺激信号产生有关,如CD2、LFA-1、VLA-4及CD28分子等。称这种分子为辅助分子或协同刺激受体分子。其中以CD28分子最为重要,已证明它的配体分子存在于B细胞或其他抗原递呈细胞上,命名为B7分子,它是50kD单体分子的穿膜蛋白,也属Ig基因超家族。B7分子在静止期B细胞、巨噬细胞或树突状细胞等表达弱,而活化型细胞表达增强。
(5)CD2分子
此分子亦称为LFA-2、LEU-5或绵羊红细胞受体等名称。为55kD单体分子,属Ig基因超家族,亦为穿膜糖蛋白分子。可存在于成熟T细胞及胸腺细胸,亦可发现于NK细胞。CD2分子是细胞间粘附分子,其配体分子称为白细胞功能相关抗原-3(LFA-3,CD58),为55~70kD糖蛋白分子,可广泛表达于造血细胞和非造血细胞。CD2分子与LFA-3分子结合可增强细胞与细胞间的粘附作用。CD2也是信号传导分子,可使T细胞活化,它不依赖于TCR途径,是T细胞活化第二途径。特别是在胸腺内早期发育阶段的胸腺细胞尚未表达TCR,此时胸腺细胞的活化与增殖可能是通过CD2分子与胸腺上皮细胞表面的LFA-3分子结合而使之活化。 由于T细胞表面具有绵羊红细胞(或其他动物)受体,故可与相应的红细胞形成E花环。 |
(6)CD44分子
CD44分子可表达于多种细胞,包括胸腺细胞、B细胞、粒细胞、巨噬细胞、红细胞、神经细胞、上皮及纤维母细胞等。CD44分子可使淋巴细胞与高内皮微静脉(HEV)结合,移行于血管、组织和淋巴细胞间,与淋巴细胞再循环密切相关,可视为一种归巢受体(homingreceptor,HR),有的T细胞比未受抗原刺激的天然T细胞可表达高水平CD44分子。
(7)细胞因子受体
细胞因子受体(cytokinereceptor,CKR)可表达于静止及活化T细胞表面,静止T细胞表面的细胞因子受体亲和力弱,数量少,而活化T细胞表面CKR亲和力高。
(8)CD45 分子
CD45分子亦称为白细胞共同抗原(leukocyte commonantigen),包括一组膜糖蛋白,CD45分子的异构体(isoforms)常限定在某些T细胞表面表达,故称之为CD45R。
(9)MHC分子
所有T细胞均表达MHC-I抗原;活化的T细胞表达MHC-II类抗原。
2、T细胞亚群的分类及功能 (1)T细胞是不均一的群体,按其抗原识别受体,可将T细胞分为二大类,一类是 TCRαβT细胞,另一类是TCRγδ T细胞。TCRαβ T细胞也是不均一的群体,根据其表型即其细胞表面的特征性分子的不同,可将成熟 T细胞分为二个亚类即 CD4+T细胞和CD8+T细胞。 ① TCRαβ T细胞和TCRγδ T细胞 二类T细胞表型分子均呈CD2+、CD3+阳性,但γδT细胞为CD4、CD8双阴性细胞(double negative cell,DN)或CD8+,而αβT细胞其表型为CD4+或CD8+,为单阳性细胞(singal positive cell,SP)。 ② CD4+T细胞 CD4+T细胞的分子表型为CD2+CD3+CD4+CD8-。其TCR识别抗原是MHC-Ⅱ类分子限制性。CD4+T细胞也是不均一的细胞群,按其功能可包括二种T细胞,即Th1和Th2。CD4+T细胞能促进B细胞、T细胞和其他免疫细胞的增殖和分化,协调免疫细胞间的相互作用。 |
③ CD8+T细胞
CD8+T细胞也是不均一的细胞群,按其功能可包括抑制性T细胞(Ts)和杀伤性T细胞(Tc)。
(2)根据TCRαβT细胞的功能可将其分为二类:一类为调节性T细胞,可包括辅助性T细胞(helper Tlymphocyte,Th)和抑制性T细胞(supperessor Tlymphocyte,Ts);另一类为杀伤性T细胞(cytolytic T cell,CTL,或Tc)。
① 辅助性T细胞(T helper,Th)
Th2主要功能是辅助B细胞,促使B细胞的活化和产生抗体。
Th1也称为迟发型超敏T细胞(delayed typehypersensitivitor),遇抗原后,可被活化增殖而释放50种以上的淋巴因子,它们可在反应的局部引起以单核细胞浸润为主的炎症,称作迟发性超敏反应(DTH),它可清除感染有慢性或胞内感染的病原体,在肿瘤免疫、移植排斥反应和自身免疫病中也有重要作用。
② 抑制性T细胞(T suppressor,Ts)
可抑制Th、Th和B 细胞的功能,由此使机体的有关淋巴细胞的增殖得到控制。
③ 细胞毒T细胞( cytotoxic Tlymphocyte,Tc)
又称杀伤性T细胞(T killercell);它能杀伤带抗原的靶细胞,例如肿瘤细胞、移植细胞或受病原体感染的宿主组织细胞等。
3、T细胞在胸腺中的发育
(1)胸腺微环境
胸腺是T细胞发育成熟的主要部位,故称之为中枢免疫器官,当T祖细胞(pro-T)自胚肝或骨髓进入胸腺后,在胸腺微环境作用下可诱导其发育分化,在其分化成熟过程中,可先后发生各种分化抗原的表达,各种细胞受体的表达,并通过正和负选择过程,最终形成T细胞库。最后成熟T细胞被迁移出胸腺,并定居于周围淋巴器官,参与淋巴细胞再循环,可分布于全身组织等一系列复杂过程。胸腺微环境主要是由胸腺基质细胞(Thymicstroma cell,TSC)、细胞外基质(extra-cellular matrix,ECM)和细胞因子等组成。
(2)T细胞在胸腺内的发育过程
T细胞在胸腺内的分化发育为三个阶段,即:
①早期T细胞发育为双阴性细胞阶段,其主要表型为CD4-和CD8-,故称为双阴性细胞(double negative,DN);
②第二阶段为不成熟胸腺细胞,由DN细胞经单阳性细胞(CD4-,CD8+)进而分化为双阳性(CD4+,CD8+)细胞(doublepositive,DP);
③第三阶段为由DP细胞选择分化为只表达CD4+或CD8+的单阳细胞(singlepositive,SP),然后迁出胸腺,移居周围淋巴器官。
T细胞T细胞在胸腺内的分化发育存在阳性选择和阴性选择:
① T细胞发育的阳性选择
② T细胞发育的阴性选择
③T细胞选择的意义:通过阳性选择获得针对抗原的反应能力;通过阴性选择获得自身耐受性;调节体内各T细胞亚群比例。
五、B淋巴细胞
B淋巴细胞是囊依赖性淋巴细胞的简称;由哺乳动物骨髓或鸟类法氏囊中的淋巴样前体细胞分化成熟而来。
B细胞的成熟发生在骨髓或法氏囊;来自骨髓的淋巴干细胞在骨髓或进入法氏囊经过阳性和阴性选择的过程发育成熟。
1、B细胞表面抗原
(1)主要组织相容性抗原(MHC)
B细胞发育未成熟时,已表达MHC-Ⅱ类分子,活化B细胞,MHC-Ⅱ类分子表达明显增多。MHC-Ⅱ类分子能增强B和T细胞间的粘附作用,同时也是递呈抗原的分子。MHC-Ⅱ类分子交联与信号传导有关,可促进B细胞的活化。近年证明超抗原可与MHC-Ⅱ类分子有高亲和性。亦与促进B细胞的活化有关。另外,B细胞是有核细胞,也表达MHC-I抗原。
(2)B细胞分化抗原(CD分子)
近年来应用单克隆抗体鉴定出存在于B细胞表面的特有抗原分子,而不存在于其他免疫细胞上。这些抗原可表达于B细胞发育分化的不同阶段,故称为分化抗原(CD),分化抗原不仅是B细胞的特异表面标志,而且具有重要的生理功能。实验证明B细胞的活化,除了由BCR与其相应抗原结合后提供活化的起始信号外,还需由其表面的辅助分子与其相应配体分子结合后,提供的协同刺激信号,才能使B细胞处于活化状态,即B细胞的活化与T 细胞一样,也是由双信号介导的。
2、B细胞表面受体
(1)B细胞抗原识别受体(BCR)
BCR是由特异识别抗原的分子和信号传导分子组成的复合分子,BCR识别抗原分子是由B细胞表面免疫球蛋白分子(surfaceimmunoglobulin,SIg或mIg)组成,它是由二条相同的重链(H)和二条相同的轻链(L)构成的4肽链分子。mIg均为单体结构,在正常外周血中多数B细胞可同时表达mIgM和mIgD,少数B细胞只表达mIgG、mIgA或mIgE。mIg是鉴别B细胞的主要特征,可用荧光标记的抗Ig抗体检测B细胞。
BCR还存在另一组分子,是由二硫键连接的异二聚分子组成,称之为Igα和Igβ链(分别命名为CD79a和CD79b)。它们的分子结构相关,功能与信号传导有关,与TCR中CD3分子的作用相似。BCR能识别可溶性蛋白抗原分子,它识别的表位是构象决定簇,这一特性与TCR明显不同。B细胞经BCR对抗原的摄取、加工和递呈作用,通过信号传导可引起胞浆内一系列生化变化及核内基因的活化、转录与表达。依其刺激的性质及B细胞分化阶段的不同,最终可导致B细胞的活化、增殖、分化、不应答或诱导细胞程序性死亡。
(2)Fc受体
许多免疫细胞表面都有 Fc受体,它是结合免疫球蛋白Fc段的分子结构。结合不同类别Ig的Fc受体,其性质各异,细胞上Fc受体的类型和数目也是不固定的。
大多数B细胞表面具有IgG Fc受体(FcγR),能与IgGFc段结合。活化B细胞此受体密度明显提高,分化至晚期又下降。FcγR可与免疫复合物结合,有利于B细胞对抗原的捕获和结合,以及B细胞的活化和抗体产生。
在活化B细胞表面可具有IgEFc(FcεRⅡ)即CD23分子,它是一种B细胞生长因子受体,可能对B细胞分化、增殖有重要作用。
抗体致敏的红细胞(EA)可B细胞结合,称为EA花环。
(3)补体受体(CR)
大多数B细胞表面有能与C3b和C3d结合的受体,分别称为CRI和CRⅡ(即CD35和CD21)。CRI主要见于成熟B细胞,活化B细胞其密度明显增高,但进入分化晚期又下降。CR可与抗原和抗体及补体形成的免疫复合物结合,促进B细胞的活化,CRⅡ也是EB病毒的受体。
抗体致敏的红细胞与补体结合(EAC)后,可与B细胞形成EAC花环。
(4)细胞因子受体(CKR)
活化B细胞可表达多种细胞因子受体,如IL-1、IL-2、IL-4、IL-5以及IFN-7等受体,与相应因子结合可促进B细胞的增殖和分化。
(5)丝裂原受体
B细胞表面的丝裂原受体与T细胞不同,故刺激B细胞转化的丝裂原也不同。如用美洲商陆(PWM)或脂多糖与外周血淋巴组织共同培养时,B细胞相应受体可与之结合而被激活,并进行增殖分化为淋巴母细胞,称为B细胞有丝分裂原反应,也称淋巴细胞转化试验,可用于对B细胞的功能检测。
六、大颗粒淋巴细胞
1、NK细胞 NK细胞来源于骨髓,主要存在于血液和淋巴样组织,特别是存在于脾中,由于其胞浆中含有颗粒故亦称为大颗粒淋巴细胞(largegranularlymphocyte,LGL)。从系统发生看,NK细胞被认为是原始杀伤T细胞,但它没有抗原识别受体,能杀伤肿瘤细胞和病毒感染细胞,所以是非特异杀伤作用,但无MHC分子的限制性,故名自然杀伤细胞。 虽然NK细胞对靶细胞的作用范围远大于杀伤T细胞,但其杀伤作用也不是随机的而是有一定范围的。NK细胞可以杀伤某些病毒感染细胞,但对正常未感染细胞无杀伤作用。NK细胞可杀伤某些肿瘤细胞株,特别是对造血细胞来源的肿瘤细胞更为敏感,但不是对所有肿瘤细胞均有作用。 从细胞表型看,NK细胞既不是T细胞也不是B细胞,NK细胞没有Ig或TCR基因重排,也不表达CD3分子。但NK细胞可表达CD2分子和低亲和性的IgGFc受体,即FcRⅡ(CD16)。如使CD2或CD16交联可促使NK细胞增殖和分泌细胞因子。值得注意的是尽管NK细胞缺乏CD3分子,但它能表达CD3的同二聚体多链分子,并与CDl6联在一起,当IgGFc与CDl6结合后,它在信号传递中也发挥重要作用。 |
NK细胞在机体内的分布较广,主要发挥抗肿瘤免疫、抗感染以及免疫调节的作用。当IgG与靶细胞结合并与NK细胞的CDl6结合时即可引起NK细胞对靶细胞的杀伤作用,称这种作用为抗体依赖的细胞介导的细胞毒性作用(ADCC)。NK细胞是ADCC的重要介导细胞,但NK细胞识别敏感靶细胞上的分子尚未明确。NK细胞可合成和分泌TNF,但无LT。在一定条件下,也可合成和分泌IFN-γ,如在T细胞缺损小鼠发现由NK细胞产生的IFN-γ可活化巨噬细胞,能杀伤感染的病原微生物。
2、K细胞
主要存在于:腹腔渗出液、血液和脾脏中,其他组织很少;无吞噬作用,但能杀伤与抗体结合的靶细胞;其表面具有IgGFc受体,可介导ADCC作用。
3、LAK细胞(lymphokine activated killer cells)
严格来说,LAK细胞并非一个独立的淋巴细胞群或亚群,而是NK细胞或T细胞体外培养时,在高剂量IL-2等细胞因子诱导下成为能够杀伤NK不敏感肿瘤细胞的杀伤细胞,称为淋巴因子激活的杀伤细胞。
七、抗原提呈细胞 抗原提呈是指细胞在其表面以能被T细胞受体(TcR)特异性识别的方式表达抗原的过程(Antigenpresent)。 是指能捕捉、加工、处理抗原,并将抗原提呈给抗原特异性淋巴细胞的一类免疫细胞(antigen-presentingcell,APC)。 抗原递呈细胞的主要功能是捕捉或处理抗原(后者如MФ),递呈抗原给T细胞或B细胞而激活之,它们有辅佐T细胞和B细胞发生免疫应答的功能;许多免疫反应的产生,如混合淋巴细胞反应,Tc的形成和T细胞依赖抗体的产生,都需要APC细胞参加。 |
1、抗原提呈细胞的分类
专职:树突状细胞、单核吞噬细胞系统、B细胞。
兼职:内皮细胞、上皮细胞、激活的T细胞。
2、树突状细胞
近几年对树突状细胞 (dendriticcell,DC)的研究,说明DC也是一种不可忽视的APC,给免疫学家提出了重新考证单核—巨噬细胞是免疫反应中主要辅佐细胞这一长期被公认的观念。将提纯的DC与单核—巨噬细胞在免疫反应中的作用进行对比实验,某些结果表明DC参加多种免疫反应,递呈抗原能力远远大于单核—巨噬细胞:①DC刺激同种混合淋巴细胞反应比B细胞、T细胞、Mφ的刺激能力至少大100倍,刺激自身混合淋巴细胞的作用亦是DC最强;②DC辅佐T细胞对破伤风类毒素的增殖反应活性可提高4~10倍;③DC在TD抗体产生过程中起辅佐作用,可以辅佐SRBC抗体的产生,还可将抗SRBC的IgM转换为IgG型。而用腹腔MФ研究对SRBC抗体产生的影响,发现MФ具有吞噬消化SRBC的能力,却抑制SRBC抗体的产生。
DC是一组非淋巴样单核细胞,其形态学特征为树突状,呈星状突起,核极不规则。这组细胞包括朗格罕氏细胞(Langerhanscell,LC)、指样交叉细胞 (interdigiting cell,IDC)、滤泡树突状细胞(folliculardendritic cell,FDC)、并指状细胞 (interdiaitating cell,IDC)。
(1)滤泡树突状细胞(follicular dendriticcell,FDC)
FDC定居于淋巴结浅皮质区淋巴滤泡生发中心内。FDC与抗原抗体复合物有高度亲合力,能够捕获和滞留抗原,并在记忆B细胞发育中起重要作用,是参与再次免疫应答的APC。
(2)淋巴样树突状细胞(lymphoid dendriticcell,LDC)
LDC主要分布在淋巴结和脾内,在移植排斥反应中起重要作用。
(3)并指状细胞(interdigitatingcell,IDC)
IDC主要定位于淋巴组织胸腺依赖区,可能由皮肤Langerhans细胞移行而来。在淋巴组织中,IDC的星状突起插入其他细胞之间,故命名为并指状细胞。它可能是淋巴结中主要的APC,并对抗原特异性T细胞具有很强刺激作用。
(4)朗格罕细胞(langerhanscell,LC)
LC位于表皮和胃肠上皮,其特征性胞内结构是胞浆中的柱状Birbeck颗粒,该颗粒参与LC抗原呈递作用的各个环节。LC是定居在皮肤中的APC,约占皮肤细胞总数的5%~10%,在介导接触性皮肤超敏反应中起关键作用。
此外,Ia+B细胞也具有抗原递呈功能,表达Ia+抗原是APC的共同特征。
DC的生物学功能:
①参与抗原提呈:利用内吞作用摄取可溶性、大颗粒或微生物抗原。
②参与T细胞发育、分化和激活:胸腺的DC对T细胞的阴性选择起重要作用;
DC还可为T细胞提供激活的协同刺激信号,对外周T细胞的分化也发挥重要作用。
③参与B细胞发育、分化及激活。
④可分泌多种细胞因子参与免疫功能的调节。
3、单核吞噬细胞系统 (1)包括: 骨髓内的前单核细胞、外周血中的单核细胞、组织内的巨噬细胞。
|
(2)Mφ的生物学作用:吞噬及细胞毒作用、抗原提呈作用、免疫调节作用(释放细胞因子)、广泛参与机体生理功能。
(3)Mφ功能的异质性:功能的复杂性、形态的差异性;不同组织器官中的Mφ具有异质性,同一组织中的Mφ具有异质性。
(4)Mφ的抗原提呈作用
进入体内的抗原,绝大部份被分解掉,只有<1%的抗原通过抗原提呈作用参与免疫反应,所以抗原的提呈是免疫反应的速率决定步骤。
所谓抗原的处理是指:巨噬细胞吞噬抗原,形成吞噬溶酶体,分解抗原成为小片断,其中某些特定的片断再和MHC分子结合,这种多肽和MHC的连结物与TCR等作用,能刺激T细胞活化。
抗原提呈作用有二种方式:
A 外在路径(exogenouspathway)
细胞外的抗原,经吞噬、分解后再和MHCⅡ分子结合,刺激 CD4+Th细胞,从而帮助B-细胞分化并产生抗体。
B 内在路径(endogenouspathway)
细胞内的抗原,如病毒感染细胞,病毒在细胞内复制,一些病毒的蛋白会和体内的MHC-Ⅰ分子结合,刺激CD8+Tc细胞分化增殖。
注意:抗原只有通过“抗原肽/MHC分子”方式才能刺激T细胞。
4、有些细胞不必经由吞噬作用也可以提呈抗原
如记忆B-细胞也可以做为抗原呈献细胞,它利用其表面免疫球蛋白(mIg)结合抗原并通过受体介导内吞作用摄入抗原,被吞入的抗原分子水解成抗原性多肽,与MHC-II类分子形成复合物,表达在B细胞表面,并提呈给CD4+T细胞。
5、兼职抗原提呈细胞
某些细胞通常不表达MHC-II分子,但在炎症过程中,或接受某些活性分子刺激后,则可表达MHC-II类分子,并能处理和提呈抗原,这些细胞被称为兼职APC。
包括:血管内皮细胞、各种上皮细胞和间质细胞、皮肤的成纤维细胞及活化的T细胞等。
兼职APC可能参与炎症反应或某些自身免疫病的发生。
八、其他免疫相关细胞
1、骨髓干细胞
2、中性粒细胞:趋化性、吞噬作用、杀菌作用、抗病毒作用和免疫调节作用。
3、嗜酸性粒细胞:对速发型超敏反应的拮抗调节作用;吞噬作用;抗寄生虫感染;产生炎症介质。
4、嗜碱性粒细胞:参与I型超敏反应,参与机体抗肿瘤免疫应答。
5、红细胞:识别和携带抗原;清除循环免疫复合物;增强吞噬作用;增强T细胞依赖性应答;免疫效应细胞作用。
九、淋巴细胞再循环
指外周淋巴器官和组织内的淋巴细胞可经淋巴管进入血流循环于全身,它们又可通过毛细血管后微静脉再回入淋巴器官或淋巴组织内,如此周而复始,使淋巴细胞从一个淋巴器官到另一个淋巴器官,从一处淋巴组织至另一处淋巴组织。这种现象称为淋巴细胞再循环。
除效应性T细胞、幼浆细胞、K细胞和NK细胞之外,大部分淋巴细胞均参与再循环,尤以记忆性T细胞和记忆性B细胞最为活跃,其中T细胞约占70-75%,B细胞为25-30%。。
参与再循环的淋巴细胞多位于淋巴器官或淋巴组织内,其总数约为血中淋巴细胞总数的数十倍,总称为淋巴细胞再循环库。淋巴细胞通过淋巴结再循环一次需18~20小时,通过脾再循环较快,约需2~8小时。一般T细胞的再循环较B细胞快。
淋巴细胞再循环的意义:可能使带有各种不同抗原受体的淋巴细胞不断地循环,有利于识别抗原,促进细胞间的协作,并使分散于全身的淋巴细胞成为一个有机的统一体。淋巴细胞一旦与相应抗原按能之后,在淋巴结或脾脏内开始发生免疫应答,经抗原刺激的T、B以及记忆细胞经再循环而散布全身并发挥功效。
 爱华网
爱华网