应医学界的朋友之邀将电子版的IPF指南放在网上供同行阅读和复制
特发性肺 (间质)纤维化诊断和治疗指南 (草案 )
中华医学会呼吸病学分会
弥漫性间质性肺疾病 (ILD)是以弥漫性肺泡单位慢性炎症和间质纤维化为主要病理特征的一大组疾病 ,特发性肺纤维化 ( IPF)是其常见类型。多年来 ,对 IPF概念的理解一直存在着差异。随着高分辨CT(HRCT)和支气管肺泡灌洗液 (BALF)检测等实验室技术的临床应用 ,特别是胸腔镜和开胸肺活检的开展,使本病从病理组织学上有了明确认识。为规范本病的诊断和治疗 ,特制定本指南 (草案 )如下。
概念
IPF 是指原因不明并以普通型间质性肺炎(UIP)为特征性病理改变的一种慢性炎症性间质性肺疾病,主要表现为弥漫性肺泡炎、肺泡单位结构紊乱和肺纤维化。UIP 不同于特发性间质性肺炎(IIP)的其它类型,如特发性脱屑性间质性肺炎/ 呼吸性细支气管炎伴间质性肺病(DIP/ RBILD)、特发性非特异性间质性肺炎(NSIP) 和急性间质性肺炎(AIP) 。
诊断要点
一、临床表现
1. 发病年龄多在中年以上,男∶女≈2∶1,儿童罕见。
2.起病隐袭,主要表现为干咳、进行性呼吸困难,活动后明显。
3.本病少有肺外器官受累,但可出现全身症状,如疲倦、关节痛及体重下降等,发热少见。
4. 50 %左右的患者出现杵状指(趾),多数患者双肺下部可闻及velcro 音。
5.晚期出现发绀,偶可发生肺动脉高压、肺心病和右心功能不全等。
二、X线胸片(高千伏摄片)
1.常表现为网状或网状结节影伴肺容积减小。随着病情进展,可出现直径多在3~15 mm 大小的多发性囊状透光影(蜂窝肺)。
2.病变分布:多为双侧弥漫性,相对对称,单侧分布少见。病变多分布于基底部、周边部或胸膜下区。
3. 少数患者出现症状时,X线胸片可无异常改变。
三、HRCT
1.HRCT扫描有助于评估肺周边部、膈肌部、纵隔和支气管2血管束周围的异常改变,对IPF的诊断有重要价值。
2.可见次小叶细微结构改变,如线状、网状、磨玻璃状阴影。
3.病变多见于中下肺野周边部,常表现为网状和蜂窝肺,亦可见新月型影、胸膜下线状影和极少量磨玻璃影。多数患者上述影像混合存在。在纤维化严重区域常有牵引性支气管和细支气管扩张,和(或)胸膜下蜂窝肺样改变。
四、肺功能检查
1.典型肺功能改变为限制性通气功能障碍,表支气管炎伴间质性肺病(DIP/RBILD)、特发性非特异性间质性肺炎(NSIP)和急性间质性肺炎(AIP)。
诊断要点
一、临床表现
1.发病年龄多在中年以上 ,男∶女≈ 2∶1,儿童罕见。
2.起病隐袭 ,主要表现为干咳、进行性呼吸困
难 ,活动后明显。
3.本病少有肺外器官受累 ,但可出现全身症状 ,如疲倦、关节痛及体重下降等,发热少见。
4.50 %左右的患者出现杵状指 (趾),多数患者双肺下部可闻及velcro音。
5.晚期出现发绀,偶可发生肺动脉高压、肺心病和右心功能不全等。
二、 X线胸片 (高千伏摄片 )
1.常表现为网状或网状结节影伴肺容积减小。随着病情进展 ,可出现直径多在 3~15mm大小的多发性囊状透光影 (蜂窝肺 )。
2.病变分布 :多为双侧弥漫性 ,相对对称,单侧分布少见。病变多分布于基底部、周边部或胸膜下区。
3.少数患者出现症状时 ,X线胸片可无异常改现为肺总量 ( TLC)、功能残气量 (FRC)和残气量 (RV)下降。一秒钟用力呼气容积 /用力肺活量 (FEV1/ FVC)正常或增加。
2.单次呼吸法一氧化碳弥散 (DLCO)降低 ,即在通气功能和肺容积正常时,DLCO也可降低。
3.通气 /血流比例失调 ,PaO2、PaCO2下降 ,肺泡气动脉血氧分压差 [P(A2a) O2 ]增大。
五、BALF检查
1. BALF检测的意义在于缩小 ILD诊断范围即排除其它肺疾病(如肿瘤、感染、嗜酸粒细胞肺炎、外源性过敏性肺泡炎、结节病和肺泡蛋白沉积症等 )。但对诊断 IPF价值有限。
2. IPF患者的 BALF中中性粒细胞 ( PMN)数增加 ,占细胞总数 5%以上,晚期部分患者同时出现嗜酸粒细胞增加。
六、血液检查
1. IPF的血液检查结果缺乏特异性。
2.可见红细胞沉降率增快 ,丙种球蛋白、乳酸脱氢酶(LDH)水平升高。
3.出现某些抗体阳性或滴度增高 ,如抗核抗体 (ANA)和类风湿因子(RF)等可呈弱阳性反应。
七、组织病理学改变
1.开胸 /胸腔镜肺活检的组织病理学呈 UIP改变。
2.病变分布不均匀 ,以下肺为重,胸膜下、周边部小叶间隔周围的纤维化常见。
3.低倍显微镜下呈“轻重不一 ,新老并存”的特点 ,即病变时相不均一,在广泛纤维化和蜂窝肺组织中常混杂炎性细胞浸润和肺泡间隔增厚等早期病变或正常肺组织。
4.肺纤维化区主要由致密胶原组织和增殖的成
纤维细胞构成。成纤维细胞局灶性增殖构成所谓的“成纤维细胞灶”。蜂窝肺部分由囊性纤维气腔构成 ,常常内衬以细支气管上皮。另外,在纤维化和蜂窝肺部位可见平滑肌细胞增生。
5.排除其它已知原因的 ILD和其它类型的 IIP。
诊断标准
诊断 IPF标准可分为有外科 (开胸 /胸腔镜)肺活检资料和无外科肺活检资料。
环境因素和风湿性疾病等所致的肺纤维化。
一、有外科肺活检资料
1.肺组织病理学表现为UIP特点。
2.除外其它已知病因所致的间质性肺疾病,如
药物、气体交换障碍。表现为限制性通气功能障碍和,肺功能异常3.(或)
4.胸片和HRCT可见典型的异常影像。
二、无外科肺活检资料(临床诊断)
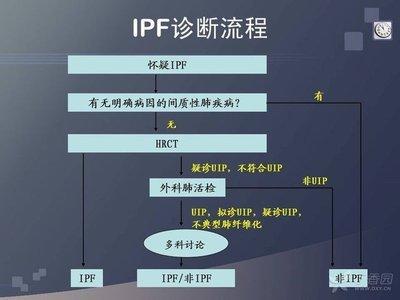
缺乏肺活检资料原则上不能确诊IPF,但如患者免疫功能正常,且符合以下所有的主要诊断条件和至少3/ 4的次要诊断条件,可临床诊断IPF。
1.主要诊断条件: (1)除外已知原因的ILD,如某些药物毒性作用、职业环境接触史和风湿性疾病等; (2)肺功能表现异常,包括限制性通气功能障碍(VC减少,而FEV1/FVC正常或增加)和(或)气体交换障碍[静态/运动时P(A2a) O2增加或DLCO降低] ;(3)胸部HRCT表现为双肺网状改变,晚期出现蜂窝肺,可伴有极少量磨玻璃影;(4)经支气管肺活检(TBLB)或BALF检查不支持其它疾病的诊断。
2.次要诊断条件: (1)年龄> 50岁;(2)隐匿起病或无明确原因进行性呼吸困难; (3)病程≥3个月; (4)双肺听诊可闻及吸气性velcro音。
鉴别诊断IPF除了与其它原因引起的ILD相鉴别外,还需要与其它类型的IIP相鉴别。IPF占所有IIP的60%以上,NSIP次之,而DIP/RBILD和AIP相对少见。均匀分布,时相一致UIP比。当AM聚积以细支气管周围气腔为主,而远端气腔不受累时,这一病理便称为RBILD。
把 UIP与其它类型 IIP区别开来至关重要,因其治疗和预后有很大区别。
一、DIP/ RBILD
1. DIP :男性多发 ,绝大多数为吸烟者。起病隐袭、干咳,进行性呼吸困难。半数患者有杵状指 (趾)。实验室检查无特殊 ,肺功能呈限制性通气功能障碍 ,弥散功能降低 ,但不如 IPF/UIP显著。影像学上早期出现双肺磨玻璃样改变 ,后期也出现线状、网状、结节状间质影像。与 UIP不同的是 DIP通常不出现蜂窝样改变。RBILD :临床表现同 DIP。杵状指 (趾)相对少见。影像学上 2/ 3患者 HRCT出现网状-结节影,未见磨玻璃影。
2. DIP显著的病理学改变是肺泡腔内肺泡巨噬细胞 (AM)均匀分布,见散在多核巨细胞。与此相伴的是轻、中度肺泡间隔增厚 与,伴少量炎性细胞浸润,无明显的纤维化和成纤维细胞灶。在低倍镜下病变
3.多数糖皮质激素治疗反应良好。
二、 AIP
1. AIP原因不明 ,起病急剧 ,临床表现为咳嗽、严重呼吸困难,继之很快进入呼吸衰竭。多数病例发病前有 “感冒”样症状,半数以上患者有发热。肺部影像学检查表现为双侧弥漫性网状、细结节及磨玻璃样阴影。急骤进展可融合成斑片乃至实变影。
2.病理表现为弥漫性肺泡损伤 (DAD)机化期改变。
3. AIP预后不良 ,死亡率极高 ,生存期很短 ,多在1~2个月内死亡。
三、 NSIP
1.可发生于任何年龄 ,男性多于女性 ,主要临床表现为咳嗽、气短,少数患者有发热。
2.影像学上表现为双侧间质性浸润影 ,双肺斑片磨玻璃阴影是本病CT特征性所见。
3.病理改变为肺泡壁明显增厚 ,呈不同程度的炎症和纤维化 ,病变时相一致 ,但缺乏UIP、DIP或 AIP的特异性改变。肺泡结构破坏较轻 ,肺泡间隔内由淋巴细胞和浆细胞混合构成的慢性炎症细胞浸润是NSIP的特点。
4.本病对糖皮质激素反应好 ,预后良好。IPF的药物治疗
一、推荐的药物和剂量
迄今,对肺纤维化尚没有一种令人满意的治疗方法。临床较常用的药物包括糖皮质激素、免疫抑制剂/细胞毒药物和抗纤维化制剂。上述药物可以单独或联合应用 ,其使用剂量和疗程应视患者的具体情况制定。推荐治疗方案为:糖皮质激素联合环磷酰胺或硫唑嘌呤 ,具体方法如下 (供参考 )。
1.糖皮质激素 :泼尼松或其它等效剂量的糖皮质激素 ,每天 0.5 mg/kg(理想体重 ,以下同 )口服 4周 ;然后每天 0.25 mg/kg,口服 8周 ;继之减量至每天 0. 125 mg/ kg或0.25 mg/kg隔天 1次口服。
2.环磷酰胺 :按每天 2 mg/ kg给药。开始剂量可为每天 25~50 mg口服,每 7~14天增加 25 mg,直至最大量 150 mg/ d。
3.硫唑嘌呤 :按每天 2~3 mg/ kg给药。开始剂量为 25~50mg/d,之后每 7~14天增加 25 mg,直至最大量 150 mg/ d。
二、疗程与疗效判定
1.疗程:(1)一般治疗3个月后观察疗效,如果患者耐受好,未出现并发症和副作用,可继续治疗至少6个月以上。(2)已治疗合用其它药物应停止治疗或改用、个月以上者6,若病情恶化,;若病情稳定或改善,应维持原有治疗。一般多主张联合用药。(3)已治疗12个月以上者若病情恶化,应停止治疗或改用、合用其它药物治疗;若病情稳定或改善,也应维持原有治疗。(4)治疗满18个月以上的患者,继续治疗应个体化。
2.疗效判定:(1)反应良好或改善:①症状减轻,活动能力增强。②X线胸片或HRCT异常影像减少。③肺功能表现TLC、VC、DLCO、PaO2较长时间保持稳定。以下数据供参考:TLC或VC增加≥10 % ,或至少增加≥200 ml ;DLCO增加≥15 %或至少增加3 ml·min21 ·mm Hg21 ;SaO2增加> 4 % ;心肺运动试验中PaO2增加≥4 mm Hg(具有2项或2项以上者认为肺生理功能改善)。(2)反应差或治疗失败:①症状加重,特别是呼吸困难和咳嗽。②X线胸片或HRCT上异常影像增多,特别是出现了蜂窝肺或肺动脉高压迹象。③肺功能恶化。以下数据供参考:TLC或VC下降≥10%或下降≥200 ml ;DLCO下降≥15 %或至少下降≥3 ml·min21 ·mm Hg -1 ;SaO2下降≥4 %,或运动试验中P(A2a) O2增加≥4 mm Hg (具有2项或2项以上者认为肺功能恶化)。
三、疗效尚不能肯定,正处于研究观察阶段的药物
1.N2乙酰半胱氨酸(NAC)和超氧化物歧化酶(SOD)能清除体内氧自由基,作为抗氧化剂用于肺
2.γ干扰素、甲苯吡啶酮、前列腺素E2以及转化生长因子等细胞因子拮抗剂,对胶原合成有抑制作用。NAC推荐大剂量(1.8 g/ d)口服。
3.红霉素具有抗炎和免疫调节功能 ,对肺纤维化治疗作用是通过抑制PMN功能来实现的。主张小剂量 (0.25 g/d)长期口服。
4.秋水仙碱 :可抑制胶原合成和调节细胞外基质 ,起到抗纤维化作用。口服剂量 0.6mg/d耐受性良好。但也有研究表明 ,秋水仙碱不能改善肺纤维化的预后。 爱华网
爱华网