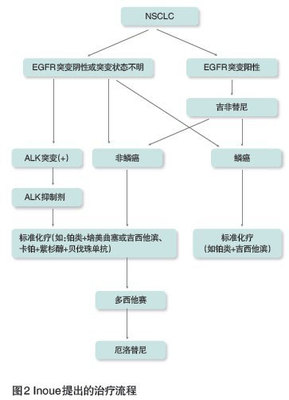
卡培他滨是已上市的第一个口服氟代嘧啶氨基甲酸酯类抗肿瘤药物,是一种细胞周期特异性抗代谢类药物,药物进入人体内经脱氧胞嘧啶酶激活后,由胞嘧啶核苷脱氨酶代谢为5-氟尿嘧啶(5-FU)。5-氟尿嘧啶作用于DNA合成期的肿瘤细胞,在一定条件下,可以阻止细胞组织分裂增生。目前,该药是用于治疗直肠癌、结肠癌、乳腺癌的新型靶向药物。
卡培他滨由瑞士罗氏公司开发,1998年4月在美国获FDA批准上市,随后陆续在瑞士等国上市。于1999年11月开始在中国进行注册临床试验,由北京、上海、广州等地的5个国家抗肿瘤药物临床试验研究中心进行临床试验,并于2001年在我国获准上市用于治疗结直肠癌和转移性乳腺癌,商品名为“希罗达(Xeloda)”。2007年,卡培他滨获得欧洲药物评价署(EMEA)批准用于胃癌的治疗。2008年,卡培他滨获得我国食品药品监督管理局(SFDA)批准,用于进展期胃癌的一线治疗。
卡培他滨的药理特点
在乳腺癌治疗方面,卡培他滨可与多西紫杉醇联合用于治疗含蒽环类药物方案化疗失败的转移性乳腺癌,亦可单独用于治疗对紫杉醇及含蒽环类药物化疗方案均耐药或对紫杉醇耐药和不能再使用蒽环类药物治疗的转移性乳腺癌患者。在治疗晚期和转移性乳腺癌方面卡培他滨效果显著。
在治疗胃肠癌方面,据世界卫生组织(WHO)统计的数据显示,2007年全球癌症新发病例超过1200万,死亡790万。其中胃癌新发病例达到94万,居人类常见恶性肿瘤的第2位,死亡约70万人。在我国,胃癌一直是高发肿瘤,每年新诊病人30多万。5-FU问世至今已经50多年,依然是消化系统肿瘤的最基本治疗药物,然而在临床应用中,由于5-FU需要静脉注射,增加了患者静脉炎、骨髓抑制、感染、出血和气胸等并发症的风险,而且提高了医疗费用。卡培他滨正是针对5-FU的不足而研发的一种肿瘤内激活的氟尿嘧啶类药物。作为口服化疗药物,卡培他滨使用方便,避免和减少静脉穿刺注射或置管的风险和并发症,可以门诊用药,减少患者住院治疗的时间,成本效益比高。
另外,其生物利用度也很高,可经小肠完整吸收,模拟了持续5-FU静脉滴注的药动学特性,符合消化道肿瘤的病理生理特点和治疗要求,还可以随时调整用药。卡培他滨独特的肿瘤细胞内激活作用机制,使其选择性地在肿瘤细胞内转变成为5-FU,在明显提高抗肿瘤活性的同时,减少全身的毒性,达到高效的靶向治疗作用,并且有助于改善生活质量。
韩国ML17032研究结果显示,卡培他滨/顺铂(XP)与5-FU/顺铂(FP)治疗AGC的无进展生存期(PFS)相似,分别为5.6和5.0个月,但XP组的客观缓解率显著高于FP组(41%对29%,P=0.03)。此外,卡培他滨口服用药的方便和安全性,不但大幅度减少了患者需要治疗的时间,也节约了医疗费用。REAL2则是迄今为止最大的有关胃食管癌的Ⅲ期临床研究,其结果显示,包含卡培他滨的三联方案组(EOX、ECX)总生存期(OS)与包含5-FU的三联方案组(EOF、ECF)相当,分别为10.9个月和9.6个月。值得注意的是,EOX方案较ECF方案显著延长OS(11.2个月对9.9个月,P=0.02)。卡西迪(Cassidy)等人荟萃分析了卡培他滨在胃肠道肿瘤中应用的6项大型随机Ⅲ期临床研究,并在2008年美国临床肿瘤学会(ASCO)第44届年会上公布了相关结果。结果表明,以卡培他滨为基础的联合方案治疗胃肠道肿瘤的OS与5-FU相当,进一步支持卡培他滨可取代5-FU成为胃肠道肿瘤治疗的核心药物。
卡培他滨的专利情况
目前卡培他滨(希罗达)尚处于专利保护期,其专利持有人为瑞士罗氏公司,在中国的注册专利号为CN1094056,专利在2013年12月17日到期。而世界专利到期日期要比中国专利早半年左右。
根据SFDA的相关规定,仿制药申报生产批文最早可在专利到期之前两年申报,即在2011年底即可开始第一批申报。
卡培他滨的药品规格及价格
目前罗氏公司在中国市场销售的卡培他滨片(希罗达)的规格和售价如下表所示。
名称 | 产地 | 规格 | 售价(元) | |
希罗达 | 上海罗氏制药 | 500mg×60片/盒 | 1190 | |
希罗达 | 上海罗氏制药 | 500mg×30片/盒 | 474 | |
希罗达 | 上海罗氏制药 | 500mg×12片/盒 | 220 |
根据希罗达的市场零售价,可估算出每片售价为15元。即,1公斤卡培他滨的价格应该约为2.5万元。(保守计算)
卡培他滨市场情况简介
抗肿瘤药物市场增长较快,IMS公司数据显示:2008年全球抗肿瘤处方药市场为482亿美元,同比增长了15.54%,占世界16大类药物市场的14.06%,比十年前的138亿美元增长了249.19%,2009年抗肿瘤处方药市场的增长率为16%以上,达到560亿美元以上。目前已有数据显示2010年保守估计全球抗肿瘤处方药物将达到600亿美元以上的销售额。据美国医药咨询公司Frost&Sullivan的统计数据显示,其中卡培他滨作为最重要的治疗乳腺癌和胃肠肿瘤药物,预计2013年专利保护到期后,全球成品药市场销售额甚至可能突破60亿美元。在我国,抗肿瘤药市场总规模2009年约为634亿元,到2010年将再增长21.47%,达到770亿元以上。前十大品种中,合资进口药品所占市场份额超50%的有吉西他滨、卡培他滨、表柔比星、利妥昔单抗、吉非替尼、厄洛替尼;其中合资进口比重最高的是卡培他滨、利妥昔单抗、吉非替尼和厄洛替尼,都占100%。从竞争格局上看,国内抗肿瘤药物生产商排名前五大的企业合计占有35%份额,上海罗氏凭借手里的3个优秀抗肿瘤品种卡培他滨、利妥昔单抗、曲妥珠单抗上升迅速,在07年就超过了恒瑞而位居第一。其中卡培他滨的贡献比重达到50%以上。2006年卡培他滨(希罗达)药物国内总体市场已达到15亿元的规模,本品单个品种(500mg*12片盒)在国内重点城市样本医院销售已达到了6980多万元,全国市场近2.5亿元;至2009年单个品种样本医院的销售额达到1.8亿元以上,总体市场规模达到40亿元以上。
生产销售卡培他滨的利润估测
2013年专利到期后,卡培他滨的市场销售量会出现一个快速增长期。据某权威制药企业的内部资料显示,保守估计全球成品年销售额将达到60亿美元,乐观估计为80亿美元以上。中国市场年销售额保守估计将增长至60-70亿人民币以上。但同时国内成品价格亦会随之下滑至大约500mg片20-25元人民币左右。根据我们现有API生产工艺,完全有能力将成本控制在8000元每公斤以内,即每500mg原料药占比重4元。加上辅料和其他成本每片大约仍有10元左右利润空间。目前一个疗程为三周,服药两周,停一周。每天平均摄入500mg片4-5片,一个疗程为48-60片,可产生480-600元利润。
竞争情况简单分析
鉴于卡培他滨在治疗乳腺癌、胃肠肿瘤方面的优异表现,快速的市场增长,广阔的市场预期,专利即将到期,同时已经列入医保等因素的影响。国内已有多家制药企业对这一品种高度关注,其中一些企业及科研院所已开始对其生产工艺进行研究。其中以江苏恒瑞、上海迪赛诺、浙江海正最具实力。本品的合成工艺具有一定的技术难度,但也并非一家独占技术。因此能否在2011年底之前完成研发和试生产任务,得到优化的生产工艺,并将全部报批资料准备完毕,赶在第一批申报,尽早投产以优势价格占领市场就成为决定成败的关键性因素。目前距离报批还有一年多一点的时间,考虑到原料合成技术已经成熟,所以现在开始准备应是最佳时机。
 爱华网
爱华网