高中化学是一门基础性、创造性和实用性的学科。下面是小编为大家整理的高中化学铝知识点,希望对大家有所帮助。
高中化学铝知识点(一)1.铝和不活动金属氧化物(主要是难熔金属氧化物如Cr2O3、V2O5以及Fe2O3等)的混合物,都叫铝热剂,在反应中铝做还原剂。反应过程放大量热,可将被还原的金属熔化成液态。
2.铝在加热时可以跟浓硫酸或硝酸反应,情况较复杂不做要求。
氧化铝与酸反应:Al2O3+3H2SO4=Al2(SO4)3+3H2O(Al2O3是两性氧化物)与碱反应:Al2O3+2NaOH=2NaAlO2+H2O ⒊氢氧化铝
① 与酸反应:Al(OH)3+3HCl=AlCl3+3H2O与碱反应: Al(OH)3+NaOH=NaAlO2+2H2O受热分解2Al(OH)3
⑵制作:溶性铝盐和氨水反应来制备Al(OH)3
AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl ( AlCl3+3NH3·H2O=Al(OH)3↓+3NH4+ )△ Al2O3+3H2O
Al2(SO4)3+6NH3·H2O=2 Al(OH)3↓+3(NH4)2SO4 ( Al3++3NH3·H2O=Al(OH)3↓+3NH4+ )
高中化学铝知识点(二)(1)铝在常温下能很快被氧化,形成致密的氧化膜,因而具有一定的抗腐蚀性。
(2)跟酸的反应
非氧化性酸:2Al + 6HCl = 2AlCl3 + 3H2↑
强氧化性酸:常温下铝遇浓硫酸或浓硝酸,会在铝表面生成致密的氧化膜而发生钝化。
(3)跟碱的反应
铝能和强碱溶液反应。该反应可理解为铝先和强碱溶液中的水反应生成氢氧化铝,氢氧化铝再和强碱反应生成偏铝酸盐:
2Al + 6H2O = 2Al(OH)3 + 3H2↑ Al(OH)3 + NaOH = NaAlO2 + 2H2O 简写为:2Al + 2H2O + 2NaOH = 2NaAlO2 + 3H2↑高温
(4)与氧化物的反应: 高温
铝热反应:2Al + Fe2O3 ==== Al2O3 + 2Fe 2Al + Cr2O3 ==== Al2O3 + 2Cr
特点: 放出大量热,使生成的金属呈液态。本质:铝从金属氧化物中夺取氧,表现出很强的还原性。 应用:焊接钢轨和冶炼某些难熔金属(如V、Cr、Mn等)。
高中化学铝知识点(三)(1)铝物理性质:密度小熔点较低,硬度较小银白色金属。 (3)化学性质:
①跟O2及其它非金属反应:铝及其化合物常温下,在空气中因生成氧化膜,具有抗腐蚀能力。
②跟某些氧化物:2Al+Fe2O323
点燃点燃
③跟水反应:2Al+6H2O → 2Al(OH)3+3H2↑ (一般不反应,只有氧化膜被破坏后反应)
④跟酸的反应:2Al+6H+→ 3Al3+ + 3H2↑(常温下,在浓H2SO4、浓HNO3中钝化)
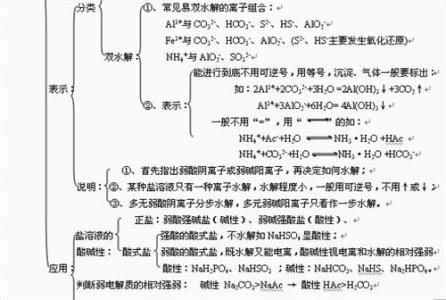
⑤跟强碱溶液反应:2Al+2NaOH+2H2O → 2NaAlO2+3H2↑
 爱华网
爱华网