前言
2008年中国糖尿病流行病学调查显示,中国20岁以上人群2型糖尿病患病率为9.7%[1]。2010年调查的全国成年人糖尿病患病率为11.6%[2]。2013年国际糖尿病联盟发布的第六版“糖尿病地图”公布[3],中国糖尿病的患病人数为9840万,居全球首位,而全球成年人糖尿病患病率为8.3%。
心血管疾病与糖尿病关系密切。2006年的“中国心脏调查”发现,慢性稳定型心绞痛和急性冠状动脉综合征的住院患者中,约80%存在不同程度的糖代谢异常,其中糖尿病占52.9%,糖尿病前期占26.4%[4]。中国医院门诊高血压患者中,糖尿病患病率为24.3% [5]。中华医学会糖尿病学分会慢性并发症调查组报告1991-2000年部分三甲医院住院的2型糖尿病患者合并高血压者占34.2%,合并其他心血管疾病占17.1% [6]。荟萃分析表明,糖化血红蛋白(HbA1c)在5%以上的患者,HbA1c每增加1%,心血管事件风险增加21%[7]。
血糖控制情况影响心血管疾病(CVD)患者预后。英国前瞻性糖尿病研究(UKPDS)提示,早期严格血糖控制对降低大血管并发症非常重要[8-9];但目前还没有足够的临床研究证明,更加严格的血糖控制(如糖化血红蛋白<6.5%)可使所有CVD合并糖尿病患者有更进一步的心血管获益。对随机对照研究如VADT[10]、ACCORD[11]、ADVANCE[12]进行的荟萃分析,也未发现口服降糖药强化治疗可降低心血管事件风险[13]。同时,强化血糖控制会增加低血糖事件发生率,低血糖可诱发合并CVD的糖尿病患者发生心肌梗死及脑卒中等。因此,重视低血糖的危害、预防,对心血管疾病合并糖尿病患者尤为重要。
为进一步提高我国心血管专科医师对心血管疾病合并糖尿病患者的综合防治能力与水平,让工作在一线的临床医师能够充分了解心血管疾病患者的糖尿病筛查流程和诊断标准、常用口服降糖药物选择以及血糖控制目标值,中国医师协会心血管内科医师分会组织心内科、内分泌科以及肾内科等领域专家,共同制订此共识。
1 心血管疾病患者糖尿病筛查流程及诊断标准
1.1 筛查对象
成年人具有下列任何一个及以上危险因素,可被定义为糖尿病高危人群,应进行糖尿病的筛查[14-15]:
(1)有糖调节受损史(定义见诊断标准);
(2) 年龄≥40岁;
(3)超重(BMI≥24 kg/m2)或肥胖(BMI≥28 kg/m2)和/或向心性肥胖
(男性腰围≥90 cm,女性腰围≥85 cm);
(4)2型糖尿病患者的一级亲属;
(5)高血压(血压≥140/90 mmHg),或正在接受降压治疗;
(6)血脂异常〔高密度脂蛋白胆固醇≤0.91 mmol/L(35 mg/dl)或甘油三酯≥2.26 mmol/L(200 mg/dl)〕,或正在接受调脂治疗;
(7)动脉粥样硬化性心脑血管疾病患者;
(8)其他: 静坐生活方式; 有巨大儿(出生体重≥4 kg)生产史,妊娠期糖尿病史;
有一过性类固醇诱导性糖尿病病史者; 多囊卵巢综合征患者; 严重精神病和/或长期接受抗抑郁症药物治疗的患者。
1.2 筛查方法
1.2.1 空腹静脉血浆血糖(FPG)
FPG是评价糖代谢状态和血糖控制水平最常用的指标,要求受试者至少空腹8小时后,在次日上午取血。仅通过FPG筛查糖尿病的优点是简便、易行,但存在漏诊的可能性。如不能确诊,且病情允许时可行口服葡萄糖耐量试验(OGTT) [4,14]。
1.2.2 口服葡萄糖耐量试验
如果FPG无法确诊糖尿病,推荐采用OGTT进行糖尿病筛查:依据FPG和负荷后2小时血糖(2hPPG)水平进行诊断。
OGTT试验方法:(1)空腹(至少8小时),在次日上午检查前,配制口服葡萄糖溶液(无水葡萄糖粉75 g,或国内常用的含 1分子结晶水的葡萄糖粉82.5 g,溶于300 ml水内)备用;(2)第一次抽血应在服糖前,前臂采血标本测定血糖。抽血时间最好是上午7:00-9:00,为第二次抽血预留充足时间。随后,应在5分钟内顺利喝完备好的口服葡萄糖溶液。第二次抽血应在服糖后2小时整,前臂采血标本测定血糖(从服糖第一口开始计时,到2小时整,为葡萄糖负荷后2小时血糖)。
注意事项:(1)试验过程中,受试者不喝茶及咖啡,不吸烟,不做剧烈运动,安静休息,但也无须绝对卧床;(2)血标本采集后应尽早送检;(3)试验前3天内,每日碳水化合物摄入量不少于150 g;(4)试验前3~7天停用可能影响血糖水平的药物,如避孕药、利尿剂或苯妥英钠等。
1.2.3 糖化血红蛋白(HbA1c)
HbA1c测定值可以反映近3个月内平均血糖水平,结果稳定、可靠、变异性小。不受进食时间、应激状态及短期生活方式改变的影响,是糖尿病监测和疗效评估的重要指标。糖尿病患者应每3~6个月监测一次。
2009年国际专家委员会和2010年美国糖尿病协会(ADA)指南均提出,将HbA1c作为糖尿病的诊断标准之一,诊断糖尿病的切点为?6.5%[16-17],糖尿病高危状态的切点介于5.7%~6.4%[16]。目前美国和欧洲已认可HbA1c在糖尿病诊断和监测中的作用。由于HbA1c检测在我国尚未实现全国标准化,并且部分医院HbA1c的检测方法未通过NGSP标准体系的认证,故HbA1c目前在我国主要用于血糖监测。世界卫生组织(WHO)的意见是,如果HbA1c检测方法通过NGSP认证,可将HbA1c作为糖尿病的诊断指标之一,以6.5%做为糖尿病的诊断切点。
考虑到我国目前存在的上述实际状况,以及中国人群中HbA1c诊断糖尿病的切点需要进一步的研究,《中国糖尿病防治指南》尚未推荐在我国采用HbA1c诊断糖尿病。
1.3 糖尿病和糖代谢异常的诊断标准[14]
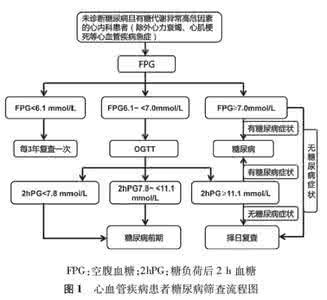
糖尿病:若有代谢紊乱症状(包括多饮、多尿、多食和不明原因的体重下降),一次FPG≥7.0 mmol/L或2hPPG≥11.1 mmol/L或随机血糖≥11.1 mmol/L,即可诊断糖尿病。无糖尿病症状者,需两次血糖值达到上述诊断标准(表1)。
糖尿病前期: 空腹血糖受损(IFG)或糖耐量受损(IGT)统称为糖调节受损(IGR,即糖尿病前期)。若FPG 6.1~<7.0 mmol/L,2hPPG<7.8 mmol/L诊断为IFG;FPG<7.0 mmol/L,2hPPG 7.8~<11.1 mmol/L诊断为IGT(表1)。
1.4 筛查流程(图1)
图1心血管疾病患者糖尿病筛查流程图
2 心血管疾病合并糖尿病患者口服降糖药物选择
2.1 常用口服降糖药物
表2总结了各种口服降糖药物的作用机理、使用方法、疗效、安全性、注意事项等主要信息。
2.1.1 双胍类:常用药物为二甲双胍,起始剂量500 mg/d,随餐服用,逐渐加量,最大剂量2000 mg/d。主要通过减少肝脏葡萄糖的输出和改善肝脏、肌肉胰岛素抵抗而降低血糖。二甲双胍可以使HbA1c下降1%~2%,并可减轻体重。单独使用二甲双胍极少发生低血糖。常见的副作用为胃肠道反应,绝大多数患者均能耐受;严重的副作用是乳酸性酸中毒。因此,禁用于肾功能不全[血肌酐水平男性>1.5 mg/dl (132.6 μmol/l),女性>1.4 mg/dl(123.8μmol/l);或肾小球滤过率<45 ml/min/1.73m2]、肝功能不全、严重感染、缺氧或接受大手术的患者。
2.1.2 胰岛素促分泌剂
2.1.2.1 磺脲类: 常用药物有格列吡嗪、格列齐特、格列喹酮及格列美脲。多从小剂量开始应用,而后根据血糖监测结果进行剂量调整。主要通过刺激胰岛β细胞分泌胰岛素,增加体内的胰岛素水平而降低血糖。磺脲类药物可以使HbA1c降低1%~2%。磺脲类药物如果使用不当可以导致低血糖,特别是老年患者和肝、肾功能不全者。磺脲类会增加体重。轻度、中度肾功能不全的患者,宜选择格列喹酮。
2.1.2.2 格列奈类:常用药物有瑞格列奈和那格列奈。多从小剂量开始应用,而后根据血糖监测结果进行剂量调整。主要通过刺激胰岛素的早时相分泌而降低餐后血糖,具有吸收快、起效快和作用时间短的特点,可降低HbA1c 0.3%~1.5%。常见副作用是低血糖和体重增加,但与磺脲类药物相比,两者的发生频率较低、程度较轻。
2.1.2.3 α-糖苷酶抑制剂:常用药物有阿卡波糖和伏格列波糖,多从小剂量开始应用,而后根据血糖监测结果进行剂量调整。通过抑制碳水化合物在小肠上部的消化和吸收而降低餐后血糖,适用于以碳水化合物为主要食物和餐后血糖升高的患者。α-糖苷酶抑制剂可使HbA1c下降0.5%~0.8%,不增加体重。单独使用时不导致低血糖,但与胰岛素促泌剂或胰岛素合用时需要注意低血糖的防治,纠正低血糖只能使用葡萄糖制剂。常见不良反应为胃肠道反应,如有疝气或曾行胃肠道外科手术应禁用。
2.1.2.4 噻唑烷二酮类:常用药物有罗格列酮和吡格列酮。每日早餐前1次服用。主要通过改善外周组织胰岛素抵抗而降低血糖。噻唑烷二酮类药物可以使HbA1c下降1%~1.5%。噻唑烷二酮类药物单独使用时不导致低血糖。但体重增加和水肿是其常见副作用。临床研究发现噻唑烷二酮类药物与骨折和心力衰竭风险增加相关。有心力衰竭(NYHA心功能II级以上)的患者、活动性肝病或转氨酶增高超过正常上限2.5倍的患者,以及有严重骨质疏松和骨折病史的患者,应禁用本类药物。
2.1.2.5 二肽基肽酶-4(DPP-4)抑制剂:目前我国上市的药物有西格列汀、维格列汀、沙格列汀、阿格列汀和利格列汀。多每日一次服用,通过抑制DPP-4而减少胰高血糖素样肽-1(GLP-1)在体内的失活,增加内源性GLP-1水平。GLP-1以葡萄糖浓度依赖的方式增强胰岛素分泌,抑制胰高血糖素分泌。临床试验显示,DPP-4抑制剂可降低HbA1c 0.5%~1.0%。DPP-4抑制剂单独使用不增加低血糖发生的风险,不增加体重。
表2常用口服降糖药物的特点[14,21-24]
2.2 口服降糖药物用药原则
2.2.1 一线药物治疗
许多国家和国际组织制定的糖尿病指南推荐:若无禁忌且能耐受,二甲双胍是2型糖尿病患者的基础用药[14、21-22]。UKPDS还显示二甲双胍可减少超重或肥胖2型糖尿病患者的心血管事件和死亡[11]。若存在禁忌或不能耐受,可考虑应用胰岛素促分泌剂或α-糖苷酶抑制剂。
如果HbA1c≥10.0%~12.0%,或血糖>16.7~19.4 mmol/L,需应用胰岛素治疗[21]。
2.2.2 联合用药
若起始HbA1c≥9%,单药治疗很难使血糖达标,需联合口服降糖药物治疗;若生活方式干预联合一线口服降糖药物单药治疗3个月不能使血糖达标,需考虑联合用药。
根据患者的情况选择联合用药方案,如胰岛素促分泌剂或α-糖苷酶抑制剂或DPP-4抑制剂或噻唑烷二酮类药物。
餐后血糖升高为主者,可优先选用格列奈类降糖药、α-糖苷酶抑制剂或DPP-4抑制剂。
若两种口服降糖药物联合治疗3个月不能使患者血糖达标,可考虑联合第三种口服降糖药物,或者联合胰岛素或GLP-1受体激动剂治疗。
3 心血管疾病合并糖尿病患者的血糖控制目标
随机对照临床试验已证实,严格的血糖控制可降低糖尿病的微血管并发症[8],但对大血管并发症的直接获益存在不同观点,有待进一步证实。早期临床研究如UKPDS报道,严格血糖控制可明显降低微血管并发症,心肌梗死风险降低16%(P=0.052);在延长观察阶段,心肌梗死和全因性死亡的风险减少13%[9]。近年,对于2型糖尿病患者的口服降糖药物强化血糖控制的随机对照研究,如VADT[10]、ACCORD[11]、ADVANCE[12],均未发现口服降糖药物强化降糖治疗可降低心血管事件风险,但对VADT、ACCORD和 ADVANCE 的心血管终点事件的综合荟萃分析后,HbA1c每下降1%,非致命性心梗相对风险降低15%,但未降低卒中或全因死亡风险[ [16]。
UKPDS研究中患者糖尿病史较短,血糖控制尤其是早期控制更为重要;而VADT、ACCORD和 ADVANCE研究中患者病史相对较长。所以对于糖尿病病程较短,无并发症的患者,强化血糖控制可带来更多的血管并发症获益;而对于病史较长,合并症较多的患者,强化血糖控制并不能带来更多的心血管获益。糖尿病治疗的目的要兼顾心血管获益和用药安全,合并CVD的糖尿病患者,一旦发生低血糖可诱发心肌梗死及脑卒中等,因而对于这类人群应尽量在避免低血糖的情况下使血糖控制达标。综合循证医学研究结果,并充分平衡风险和血管获益,结合患者的年龄、糖尿病病程以及CVD病史等,将血糖控制目标个体化[11、19、21]。
糖尿病患者的血糖控制可根据自我血糖监测(SMBG)的结果和HbA1c水平综合判断。在治疗之初或血糖未达标时,应每3个月进行一次HbA1c的测定,血糖控制达标者至少每半年进行一次HbA1c的测定。
(1)已证实HbA1c<7.0%可减少糖尿病患者微血管并发症,故推荐血糖控制目标:HbA1c<7.0%,FPG<7.0 mmol/L,餐后2小时血糖(2hPG)<10 mmol/L。
(2)糖尿病病史较短、预期寿命较长、没有并发症的患者,在不发生低血糖的情况下可考虑将HbA1c控制至6.5%以下。
(3)有严重低血糖病史,或预期寿命较短,或有显著微血管或大血管并发症的患者,可放宽血糖目标值:HbA1c<7.5%-8.0% 。
(4)慢性疾病终末期(如心功能NYHA Ⅲ-Ⅳ级、慢性肾功能不全、恶性肿瘤伴转移、中-重度认知功能障碍等)患者的HbA1c可放宽至<8.5%。
4 特殊情况说明
4.1 心血管疾病
4.1.1 急性冠脉综合征(ACS)
若血糖>10.0 mmol/L,可使用以胰岛素为基础的治疗方案 [19,25-26],使血糖水平控制在7.8~10 mmol/L,同时注意避免低血糖发生[27]。
应激情况下可出现暂时性血糖升高,对于既往没有糖尿病病史(特别是HbA1c在正常范围者),不能以此血糖值诊断糖尿病,须在应激消除后复查,必要时行OGTT明确[14]。
4.1.2 经皮冠状动脉介入治疗(PCI)
以往接受PCI的患者使用对比剂之前需停用二甲双胍的建议,缺乏足够的循证医学证据。因此,使用对比剂前可不停用,但需密切监测肾功能,若肾功能恶化,应立即停用二甲双胍[18-20]。
4.1.3 冠状动脉旁路移植术(CABG)
围手术期不推荐口服降糖药,应使用胰岛素治疗[18]。
4.1.4 心力衰竭
急性心力衰竭伴有缺氧情况,禁用双胍类药物、噻唑烷二酮类药物。对于慢性心力衰竭患者,需根据肾功能、血氧状态以及基础心功能等情况,选择应用口服降糖药物,还应注意监测血清乳酸水平和血气分析指标。心功能NYHAⅡ~Ⅳ级的患者,应避免使用噻唑烷二酮类药物[28]。DPP-4抑制剂在心功能NYHA Ⅱ-Ⅲ级临床经验有限,Ⅲ-Ⅳ级无临床经验,故心力衰竭时应慎用或禁用。目前缺乏其他药物在心力衰竭患者中的用药证据。
4.2 肾功能不全
心血管疾病和糖尿病患者常合并慢性肾脏病(CKD),而CKD患者应基于药物的药代动力学特征和患者的肾功能水平综合判断,选择合适的降糖药物,并适当调整剂量,确保在有效降糖的同时不增加低血糖风险。
瑞格列奈、利格列汀在肾功能不全时无需调整剂量;二甲双胍在GFR 45-59 ml/min/1.73m2时应减量,GFR<45 ml/min/1.73m2禁用;ɑ-糖苷酶抑制剂在GFR <30 ml/min/1.73m2时禁用。其他药物在肾功能不全中的应用详见图2。
4.3 阻塞性睡眠呼吸暂停综合征(OSAHS)
对于OSAHS 伴发2型糖尿病的患者, 常用降糖药物均可选用,但应尽可能使用不增加体重的药物。由于OSAHS 易发生夜间缺氧, 对于低氧血症严重者慎用或禁用双胍类药物。
4.4 老年糖尿病患者
老年患者降糖目标应个体化,考虑个人功能状态、共患或伴发疾病,尤其应考虑是否发生过心血管疾病、低血糖、微血管并发症等。生活自理的老人,HbA1c为7.0%~7.5%;生活无法自理者,以8.0%为宜;对于虚弱患者,可放宽至8.5%[31]。
老年糖尿病患者病情复杂、发生并发症或合并症的风险高、器官功能逐渐衰退。因此,对于老年糖尿病患者而言,治疗方案需更有针对性、更符合个体情况、更重视安全性。
4.5 低血糖[32]
糖尿病患者血糖水平低于3.9 mmol/L(70 mg/dl)时,定义为低血糖。
在口服降糖药物中,胰岛素促泌剂均可引起低血糖,其中磺脲类药物尤为常见,格列奈类药物因其药理作用时间短,相对较少见。
常见原因包括:药物剂量、剂型或给药时间,甚至治疗方案需要调整,均可能与低血糖相关;过强的身体运动使肌肉等外周组织对葡萄糖摄取和利用增加,而消耗血糖;未正常进食,或隔夜禁食时间偏长等,导致食物来源的外源性葡萄糖摄入减少或延迟所致;因肾功能不全等疾病,使体内胰岛素或胰岛素促泌剂清除能力下降,血中胰岛素或胰岛素促泌剂浓度过高,血糖被过度降低。
二甲双胍、α-糖苷酶抑制剂、噻唑烷二酮类及DPP-4抑制剂单独使用时一般不会导致低血糖。
结语
糖尿病与心血管疾病关系密切,糖尿病是心血管疾病的主要危险因素之一,其主要死亡原因是心血管疾病。血糖管理是心血管疾病综合防控的重要内容之一。心血管专科医师应熟练掌握心血管疾病合并糖尿病患者常用口服降糖药物的应用原则。
专家组成员名单(按姓氏汉语拼音为序):董吁钢(中山大学附属第一医院心血管内科);郭艺芳(河北省人民医院老年病一科);高颖(首都医科大学附属北京同仁医院心脏中心);何奔(上海交通大学医学院附属仁济医院心血管内科);洪天配(北京大学第三医院内分泌科);胡大一(北京大学人民医院心脏中心);姜红(中日友好医院心脏内科);蒋捷(北京大学第一医院心血管内科);李虹伟(首都医科大学附属友谊医院心脏中心);李建军(中国医学科学院阜外心血管病医院二十五B病区血脂异常与心血管病诊治中心);李凌(郑州大学第一附属医院心血管内科);李全民(中国人民解放军第二炮兵总医院内分泌科);李新立(南京医科大学第一附属医院心血管内科);李勇(复旦大学附属上海华山医院心血管内科);刘梅林(北京大学第一医院老年病内科);卢永昕(华中科技大学同济医学院附属协和医院心血管内科);马长生(首都医科大学附属北京安贞医院、同仁医院心脏中心);谌贻璞(首都医科大学附属北京安贞医院肾内科);孙宁玲(北京大学人民医院心脏中心);唐梅(首都医科大学附属北京友谊医院干保中心老年心内科);汪道文(华中科技大学同济医学院附属同济医院心血管内科);吴平生(南方医科大学南方医院心血管内科);严晓伟(北京协和医院心血管内科);杨光燃(首都医科大学附属北京同仁医院内分泌科);杨萍(吉林大学中日联谊医院心血管内科);叶平(中国人民解放军总医院老年心内科);郑杨(吉林大学第一医院心血管疾病诊治中心);周迎生(首都医科大学附属北京安贞医院内分泌代谢科
 爱华网
爱华网