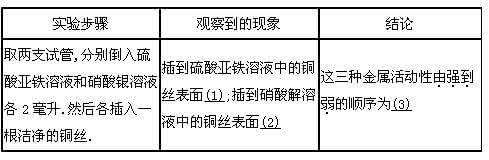
一、解答题(共12小题,满分0分)1.H7N9型禽流感是一种新型禽流感,于2013年3月底在上海和安徽两地率先发现,已经造成多人死亡,帕拉米韦是一种新型的抗流感病毒药物,属神经氨酸酶抑制剂,对抑制H7N9禽流感有一定的效果,其化学式为:C15H28N4O4(其相对分子质量为328),回答以下问题:
(1)帕拉米韦是由四种元素组成.
(2)帕拉米韦中H、N两种元素的质量比为:1:2.
(3)帕拉米韦中碳元素的质量分数为:54.9%. 显示解析2.如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
(1)t1°C时,A、B两种物质的溶解度是A<B(填“>”、“<”或“=”,下同).
(2)将t3°C的A、B两种物质的饱和溶液各200g,降温至t1°C,析出晶体的质量关系是A>B.
(3)t2°C时,100g水中溶解50gA刚好饱和,那么50g水中溶解25gB也刚好达饱和,此时溶液的质量分数是33.3%(精确到0.1%). 显示解析3.某实验需要100g8%硫酸铜溶液.
(1)该溶液的溶质质量是8g,从中取10g溶液,此溶液中溶质的质量分数是8%.
(2)实验室用硫酸铜晶体(分子式为:CuSO4.5H2O)配置100g 8%的硫酸铜溶液,需称取硫酸铜晶体12.5g.(已知相对分子质量:CuSO4.5H2O为250,CuSO4为160)VIP显示解析4.某兴趣小组用10g镁条与溶质质量分数为49%的稀硫酸反应.测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质).
(1)当稀硫酸的质量为70g,产生的氢气的质量为0.5g.
(2)用化学方程式说明当稀硫酸的质量为10g时,为什么不产生氢气MgO+H2SO4=MgSO4+H2O.
(3)计算镁条中镁元素的质量分数(写出计算过程).VIP显示解析5.小亮同学对在空气中放置一段时间的“铜树”(铝丝浸泡在硫酸铜溶液中制成,如图)的成分进行分析,取出64.1g固体样品,用10%的盐酸充分溶解,溶液呈无色,产生的气体和剩余固体随消耗10%的盐酸质量变化关系曲线如图:
结合图中数据分析:
(1)读图可知,Cu元素的质量32g,64.1g“铜树”有Cu、Al、Al2O3(填化学式).
(2)请结合化学方程式计算该“铜树”中Al元素的质量分数.
(3)只知道“铜树”质量m1和消耗10%的盐酸总质量(m2),也能求出“铜树”中铝元素的质量分数,其表达式为9×m2×10%36.5gm1×100%(用m1和m2表示,可不化简).VIP显示解析6.实验室有一瓶未知浓度的BaCl2溶液,某同学取出150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液.反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图所示.已知:BaCl2+Na2CO3=BaCO3↓+2NaCl
请计算:
(1)配制26.5%的Na2CO3溶液80g,需要Na2CO3固体21.2gg.
(2)BaCl2溶液的溶质质量分数是多少?(写出计算过程,结果保留到0.1%) 显示解析考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.专题:压轴实验题;溶液的组成及溶质质量分数的计算;有关化学方程式的计算.分析:(1)根据溶质质量分数的计算公式知道溶液质量和溶液质量分数能求配制该溶液的所需固体质量.
(2)向BaCl2溶液滴加Na2CO3溶液,二者能发生复分解反应生成沉淀,其方程式为:BaCl2+Na2CO3=BaCO3↓+2NaCl,根据题给数据及图示,利用化学方程式求得BaCl2溶液的溶质质量分数.解答:解:(1)配制26.5%的Na2CO3溶液80g,需要Na2CO3固体的质量为:80g×26.5%═21.2g
(2)从图中获知,当BaCl2完全转化为沉淀时消耗Na2CO3溶液的质量为40g.
设BaCl2的质量为 x,则
BaCl2+Na2CO3=BaCO3↓+2NaCl
208 106
x 40g×26.5%
208106=x40g×26.5%
解得:x=20.8g
该BaCl2溶液的溶质质量分数=20.8g150g×100%=13.9%
答:该BaCl2溶液的溶质质量分数为13.9%.点评:考查溶液和化学反应融合的题目,是综合性的题型,要求比较高.通常学生在计算时常常会忽视了实际参加反应的是溶液中溶质的质量,而往往会把40g直接代入化学方程式进行计算.这就要求学生足够细心、会分析、且条理分明.7.现有HCl与CaCl2的混合溶液,为了分析混合溶液中HCl和CaCl2的质量分数,设计了如下实验方案:
【实验数据】实验共记录了两组数据:
第①组,气体吸收完全后,NaOH溶液质量增加4.4g;
第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
(1)混合溶液中HCl的质量分数为7.3%.(只写结果)
(2)混合溶液中CaCl2的质量分数为多少?(写出计算过程)
(3)实验中混合溶液与Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为8.2%.(不考虑过滤中的损失.只写结果,保留小数点后一位)
(4)若在100g混合溶液中不断加入10.6% 的Na2CO3的溶液,请你画出加入Na2CO3溶液的质量与产生沉淀的质量的关系图.(在答题卡的坐标图中作图)
VIP显示解析8.过氧化钠(Na2O2)是一种重要的氧化剂,它与水反应产生氧气的化学方程式为:2Na2O2+2H2O═4NaOH+O2↑.现将一定量的Na2O2加入盛有87.6g水的烧杯中,完全反应后,称得溶液的质量比反应前过氧化钠和水的总质量减少了3.2g(假定水蒸气的挥发忽略不计).请回答:
(1)反应生成氧气的质量为3.2g.
(2)计算反应后所得溶液中溶质的质量分数.(写出详细的计算过程) 显示解析考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.专题:溶质质量分数与化学方程式相结合的计算.分析:(1)根据质量守恒定律可以知道反应前后减少的质量即为氧气的质量;
(2)根据反应的化学方程式可以知道反应后的溶液为氢氧化钠溶液,可以根据氧气的质量结合化学方程式求算出氢氧化钠的质量,进而求算出氢氧化钠溶液的质量分数.解答:(1)根据质量守恒定律可以知道反应前后减少的质量即为氧气的质量,即生成氧气的质量为3.2g.
(2)解:设参加反应的过氧化钠的质量为x,生成氢氧化钠的质量为y.
2Na2O2+2H2O═4NaOH+O2↑
156 160 32
x y 3.2 g
156x=323.2g,160y=323.2g
解得x=15.6 g,y=16 g
反应后所得溶液中溶质的质量分数=16g87.6+15.6g?3.2g×100%=16%
故答案为:(1)3.2;(2)答:反应后所得溶液中溶质的质量分数16%.点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景,结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地解答即可9.实验室新进一批块状大理石.某化学小组成员称取12.5g该大理石样品,加入足量稀盐酸测定碳酸钙的含量.完全反应后,称得固体剩余物的质量为2.5g.样品中杂质不溶于水且不与稀盐酸反应,请回答下列问题:
(1)该样品中碳酸钙的质量为10g.
(2)计算12.5g该样品最多可以制得二氧化碳的质量,写出必要的计算过程. 显示解析考点:根据化学反应方程式的计算.专题:压轴实验题;有关化学方程式的计算.分析:(1)样品中杂质不溶于水且不与稀盐酸反应,所以加入足量稀盐酸完全反应后固体剩余物的质量2.5g即是杂质的质量,碳酸钙的质量=12.5g-2.5g=10g;
(2)据碳酸钙的质量结合方程式计算二氧化碳的质量.解答:解:(1)样品中杂质不溶于水且不与稀盐酸反应,所以加入足量稀盐酸完全反应后固体剩余物的质量2.5g即是杂质的质量,碳酸钙的质量=12.5g-2.5g=10g;
(2)设12.5g该样品最多可以制得二氧化碳的质量的为x,12.5g该样品中碳酸钙的质量为12.5g-2.5g=10g;
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
10g x
10010g=44x
x=4.4g
故答案为:(1)10g;(2)12.5g该样品最多可以制得二氧化碳4.4g.点评:本题难度不是很大,主要考查了学生分析题意获取选项及根据化学方程式进行有关的计算,培养学生分析问题的能力和解决问题的能力.10.某兴趣小组从废铝锅底部剪一块铝片,将它放入21.9%的稀盐酸中,产生氢气的质量与消耗盐酸的质量如图所示(假设酸与氧化膜反应时没有H2产生,其它杂质不与酸反应),请回答:
(1)从图中看出,该反应产生了H21.2g.
(2)产生氢气的化学方程式为:2Al+6HCl═2AlCl3+3H2↑;铝片中铝单质的质量为10.8g.
(3)求被氧化的铝的质量占未氧化时铝片总质量的质量分数,写出计算过程. 显示解析考点:根据化学反应方程式的计算.专题:学科交叉型;压轴实验题;利用图像,进行分析计算;有关化学方程式的计算.分析:(1)图象为产生氢气质量随所加盐酸质量变化情况.根据图象可知,放出氢气质量为1.2g;
(2)未被氧化的铝与盐酸发生置换反应,可以生成氯化铝和氢气;由反应放出氢气的质量,根据反应的化学方程式,计算与酸反应的铝片的质量;
(3)根据产生氢气的图象,当加入50.0g稀盐酸时开始与铝片发生反应,直到加入250.0g盐酸时恰好完全反应.由与氧化铝反应所消耗盐酸的质量,根据反应的化学方程式计算氧化铝的质量,由氧化铝中铝元素的质量分数求得被氧化的铝的质量,最后使用被氧化的铝的质量被氧化的铝的质量+未被氧化的铝的质量×100%计算出被氧化的铝的质量占未氧化时铝片总质量的质量分数.解答:解:(1)根据产生氢气的质量与消耗盐酸的质量图,可得生成氢气质量为1.2g;
故答案为:1.2;
(2)未变质的铝与盐酸发生置换反应,生成氯化铝和氢气,反应的化学方程式为2Al+6HCl═2AlCl3+3H2↑;
设与200.0g盐酸反应的铝的质量为x
2Al+6HCl═2AlCl3+3H2↑
54 219
x 200.0g×21.9%
54x=219200.0g×21.9% x=10.8g
故答案为:2Al+6HCl═2AlCl3+3H2↑;10.8;
(3)根据图象,与氧化铝反应的盐酸的质量为50.0g;设氧化铝的质量为y
Al2O3+6HCl═2AlCl3+3H2O
102 219
y 50.0g×21.9%
102y=21950.0g×21.9% y=5.1g
被氧化的铝的质量=5.1g×27×227×2+16×3×100%=2.7g
被氧化的铝的质量占未氧化时铝片总质量的质量分数=2.7g2.7g+10.8g×100%=20%
答:被氧化的铝的质量占未氧化时铝片总质量的质量分数为20%.点评:解答此类问题的根本点在于对反应图象的曲线进行分析,曲线起点表示开始与铝发生反应放出氢气,曲线的折点表示此时恰好完全反应.11.氯化镁是制取镁的原料之一.现要测定某化工产品(含MgCl2和KCl)中所含的氯化镁质量分数,进行实验:先将10g样品完全溶于水,然后把50g一定质量分数的氢氧化钾溶液平均分五次加入样品溶液中,充分振荡,实验所得数据见下表:
编号12345加入氢氧化钾溶液的质量/g1010101010生成沉淀的质量/g0.58a1.742.322.32请分析上述数据,回答下列问题:
(1)表中a为1.16.
(2)样品中的氯化钾属于化肥中的钾肥,可回收利用.
(3)所用的氢氧化钾溶液中溶质的质量分数是11.2%.
(4)计算样品中氯化镁的质量分数是多少?(写出计算过程) 显示解析考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算;常见化肥的种类和作用.专题:压轴实验题;综合计算(图像型、表格型、情景型计算题).分析:(1)对比表中前三组的数据可以得出X的值.
(2)含有氮元素的肥料称为氮肥.含有磷元素的肥料称为磷肥.含有钾元素的肥料称为钾肥.同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥.
(3)分析表格可以发现,当生成0.58克沉淀时,氢氧化钾溶液中氢氧化钾全部参加反应;可求得10g氢氧化钾溶液中溶质氢氧化钾的质量,进一步可求得氢氧化钾溶液中溶质的质量分数
(4)由生成沉淀的总质量根据氯化镁与氢氧化钠反应的化学方程式可以计算出氯化镁的质量,进而计算出样品中氯化镁的质量分数.解答:解:(1)由表中1、3两次的数据可知,10g氢氧化钾溶液与氯化镁反应能生成0.58g沉淀,因此20g氢氧化钠溶液能生成1.16g沉淀.
(2)氯化钾提供的主要营养元素是钾元素,属于钾肥.
(3)设10g氢氧化钾溶液中溶质氢氧化钾的质量为x.
MgCl2+2KOH═2KCl+Mg(OH)2↓
112 58
X 0.58克
112X=580.58g
X=1.12g
氢氧化钾溶液中溶质的质量分数为:1.12g10g×100%═11.2%
答:氢氧化钾溶液中溶质的质量分数为11.2%
(4)设原混合物中含有MgCl2的质量为x.
MgCl2+2KOH=Mg(OH)2↓+2KCl
95 58
x 2.32g
9558=x2.32g,x=3.8g
则样品中氯化镁的质量分数是3.8g10g×100%=38%
答:样品中氯化镁的质量分数是38%点评:本题是一道有关物质组成的综合计算题,包括根据化学方程式的计算,有关溶液中溶质质量分数的计算,考查了学生根据实验数据分析反应情况的能力.12.现有一种碱性调味液,是碳酸钠和氯化钠组成的溶液.为了测定碱性调味液中碳酸钠和氯化钠的质量分数,设计了如下实验方案.
【实验一】取三份碱性调味液各100g,分别缓慢加入到20g、40g和60g某盐酸中,测得三组实验数据见下表(气体的溶解忽略不计):
第Ⅰ组第Ⅱ组第Ⅲ组盐酸的质量/g204060生成气体的质量/s2.24.45.5根据实验及有关数据进行分析与计算:
(1)100g碱性调味液与盐酸完全反应生成气体的质量为5.5g.
(2)碱性调味液中碳酸钠的质量分数为多少?(写出计算过程)
(3)100g碱性调味液与该盐酸反应后溶液pH=7时,需要盐酸的质量为50g
【实验二】在上述第Ⅲ组反应后的溶液中加AgNO3溶液,测得实验数据见下图:
根据实验及有关数据进行分析:
(4)某同学计算出碱性调味液中氯化钠的质量分数为20.5%(保留到小数点后一位)后经检查无数字运算错误.请判断该计算结果是否正确,如不正确要指出错误原因.不正确.把碳酸钠与盐酸反应生成的氯化钠的质量没有减去. 显示解析考点:含杂质物质的化学反应的有关计算.专题:压轴实验题;溶质质量分数与化学方程式相结合的计算.分析:(1)根据实验数据分析可知20克稀盐酸完全反应生成二氧化碳的质量,据此可算出60克稀盐酸完全反应生成二氧化碳的质量,进而根据第三组实验数据可知100g碱性调味液与盐酸完全反应生成气体的质量.
(2)根据二氧化碳的质量可算出碳酸钠的质量,再根据碳酸钠的质量碱性调味液的质量×100%可求出碱性调味液中碳酸钠的质量分数.
(3)根据实验数据分析可知参加反应的盐酸与生成的二氧化碳的质量比关系,据此可求出所需要的盐酸的质量.
(4)先计算出碱性调味液中氯化钠的质量分数,判断该计算结果是否准确,然后根据计算结果分析错误原因.求碱性调味液中氯化钠的质量分数的方法是:沉淀为氯化银,包括剩余盐酸与硝酸银反应生成的氯化银和氯化钠与硝酸银反应生成的氯化银.先求出剩余盐酸中溶质的质量,根据剩余盐酸中溶质的质量求出和盐酸反应生成的氯化银的质量,进而求出和氯化钠反应生成的氯化银的质量,利用氯化钠和硝酸银反应的化学方程式,根据氯化银的质量求出氯化钠的质量,此氯化钠包括反应生成的氯化钠和原混合物中的氯化钠,用总氯化钠的质量-反应生成的氯化钠的质量即为碱性调味液中氯化钠的质量,最后根据氯化钠的质量碱性调味液的质量×100%即可求出碱性调味液中氯化钠的质量分数.解答:解:
(1)根据前两组实验数据分析可知每20克盐酸完全反应生成2.2克二氧化碳,则60克盐酸完全反应应生成6.6克二氧化碳,在第三组实验中加入60克盐酸只生成5.5克二氧化碳,说明第三组实验中盐酸有剩余,碳酸钠反应完,所以100g碱性调味液与盐酸完全反应生成气体的质量为5.5克.故答案为:5.5
(2)设与盐酸反应的碳酸钠的质量为x.
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
x 5.5g
106x=445.5g
x=13.25g
碱性调味液中碳酸钠的质量分数=13.25g100g×100%=13.25%
答:碱性溶液中碳酸钠的质量分数为13.25%.
(3)根据实验数据分析可知每生成1.1克二氧化碳参加反应的盐酸的质量为10克,现在共生成5.5克二氧化碳,参加反应的盐酸的质量为50克.故答案为:50
(4)设20克盐酸中溶质的质量为y
Na2CO3+2HCl=2NaCl+CO2↑+H2O
73 44
y 2.2g
73y=442.2g
y=3.65g
所用盐酸中溶质的质量分数=3.65g20g×100%=18.25%
第Ⅲ组反应后的溶液中含氯化氢的质量=10g×18.25%=1.825g
设和盐酸反应生成的氯化银的质量为z
HCl+AgNO3═AgCl↓+HNO3
36.5 143.5
1.825g z
36.51.825g=143.5z
z=7.175g
和氯化钠反应生成的氯化银的质量=57.4g-7.175g=50.225g
设氯化钠的总质量为a
NaCl+AgNO3═AgCl↓+NaNO3
58.5 143.5
a 50.225g
58.5a= 143.550.225g
a=20.475g
设反应生成的氯化钠的质量为b
Na2CO3+2HCl=2NaCl+CO2↑+H2O
117 44
b 5.5g
117b=445.5g
b=14.625g
碱性调味液中氯化钠的质量=20.475g-14.625g=5.85g
碱性调味液中氯化钠的质量分数=5.85g100g×100%%=5.85%
因而该计算结果不对,该计算结果为20.5%,根据上述计算可知,把碳酸钠与盐酸反应生成的氯化钠的质量没有减去时算出的结果是20.5%.
故答案为:不正确.把碳酸钠与盐酸反应生成的氯化钠的质量没有减去
(或把碳酸钠与盐酸反应生成的氯化钠的质量也计算进去了)点评:解答本题可用数据分析法,即解题时正确分析数据,找出数据的变化特征及彼此之间的关系,将综合复杂的问题分解为简单的计算,从而顺利解题.
 爱华网
爱华网