昨天我们复习了有关氧气的一些知识,今天我们来看下二氧化碳的考点都有哪些吧。如果您觉得好,请关注此微信号,并且分享出去,您的支持将是我的动力!
考试内容
考试要求
要求层次
空气
二氧化碳
1.说明二氧化碳的主要性质和用途
★★★
2.用二氧化碳的性质解释一些常见的现象
★★★
基本实验
1.能用简单的装置和方法研究二氧化碳的性质
★★
2.能用简单的装置和方法制取二氧化碳
★★
4.会检验二氧化碳
★★★
我们还是来看看二氧化碳在中考说明中是怎么说的
考点一:说明二氧化碳的主要性质和用途(★★★)
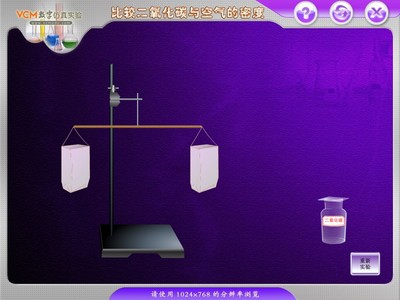
1、物理性质:无色,无味的气体,密度比空气大,能溶于水,高压低温下可得固体----干冰(因此干冰是固态的二氧化碳)
2、化学性质:
A、一般情况下不能燃烧,也不支持燃烧,不能供给呼吸
B、与水反应生成碳酸:
CO2 H2O=H2CO3
生成的碳酸能使紫色的石蕊试液变红,碳酸不稳定,易分解
H2CO3 = H2O CO2↑
C、能使澄清的石灰水变浑浊:
CO2 Ca(OH)2=CaCO3↓ H2O
用于检验二氧化碳;这也是久置装石灰水的试剂瓶壁有一层白膜的原因。要除去这白膜,用稀盐酸。其原理是
CaCO3 2HCl=CaCl2 H2O CO2↑
D、与灼热的碳反应:
考点二:用二氧化碳的性质解释一些常见的现象(★★★)
A、灭火:既利用其物理性质——密度比空气大;又利用其化学性质——不能燃烧,也不支持燃烧
B、干冰可用于人工降雨、制冷剂——利用干冰升华时要吸收大量的热
C、温室肥料——二氧化碳能让植物进行光合作用(利用化学性质)
D、做碳酸型饮料——利用二氧化碳能溶于水
考点三:能用简单的装置和方法制取二氧化碳(★★)
1、药品:大理石与稀盐酸
A、不能用H2SO4 与CaCO3反应的原因:生成的CaSO4微溶于水,会覆盖在CaCO3表面,阻止反应的进行。
B、不能用HCl与Na2CO3(碳酸钠)粉末反应的原因:Na2CO3与盐酸反应速率快,不利于收集。
2、原理:用石灰石和稀盐酸反应:
CaCO3 2HCl=CaCl2 H2O CO2↑
3、装置图
装置的注意事项:若用长颈漏斗来注入盐酸,长颈漏斗下端必须伸入液面以下(这个操作叫液封,他的目的是防止生成的气体从长颈漏斗漏出),分液漏斗则不用
4、气体收集方法:向上排空气法——原因:密度比空气大,能溶于水
考点四:会检验二氧化碳(★★★)
检验:将制得的气体通入澄清的石灰水,如果变浑浊,则是二氧化碳。
验满:用点燃的木条,放在集气瓶口,如果木条熄灭。证明已集满二氧化碳气体。
本文为化学之路原创修改,若转载请联系作者
 爱华网
爱华网