陷阱1:忽视气体摩尔体积适用的条件。22.4L·mol-1指在标准状况下(0 ℃,101kPa)的气体摩尔体积。若题中出现物质的体积,需考虑所给物质的状态是否为气体,条件是否为标准状况。
陷阱2:忽视物质的聚集状态。气体摩尔体积适用的对象是气体(包括混合气体)。一些在标准状况下是液体或固体的物质,如CCl4、SO3、己烷、苯常作为干扰因素迷惑考生。另外注意烃的衍生物中CH3Cl、HCHO等在标准状况下为气体。
陷阱3:忽视对物质微观结构的判断。(1)注意某些物质分子中的原子个数,如Ne、O3、白磷等。(2)特殊物质的摩尔质量或分子中的中子数,如D2O、T2O、18O2等;(3)一些物质中的化学键数目,如SiO2、Si、CH4、P4、CO2、C60、烃中化学键的数目等。
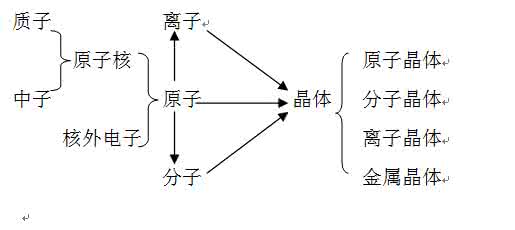
陷阱4:忽视电解质溶液中电离与水解的影响。注意弱电解质的电离及离子的水解,如1 molCH3COOH溶于水时,溶液中CH3COO-的物质的量小于1mol;1 mol FeCl3溶于水时,由于Fe3+的水解,溶液中Fe3+ 的物质的量小于1 mol。
陷阱5:忽视对氧化还原反应中电子转移数目的分析。较复杂的氧化还原反应中,需正确求算电子转移的数目,如Na2O2+ H2O,Cl2 + NaOH,电解AgNO3溶液等。
陷阱6:忽视分散系的变化导致微粒数目的变化。如FeCl3溶液转化为Fe(OH)3胶体,因为胶体微粒是分子的集合体,所以胶粒的数目小于原溶液中Fe3+的数目。
陷阱7:忽视可逆反应不能进行到底。如NO2和N2O4的相互转化,合成氨反应等。
【例】(2011·江苏卷)设NA为阿伏加德罗常数的值。下列叙述正确的是
A.1 mol甲醇中含有C-H键的数目为4NA
B.25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA
C.标准状况下,2.24 L己烷含有分子的数目为0.1NA
D.常温常压下,Na2O2 与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4 NA
【解析】熟练掌握阿伏加德罗常数并能识别正误判断的陷阱是正确解题的关键。A项,甲醇的结构式为,1mol甲醇中含有C—H键的数目为3NA,不正确;B项,溶液的体积未知,无法计算溶质的物质的量;C项,标准状态下己烷不是气态物质,不正确。答案:D。
 爱华网
爱华网