avid Kohn 发表于 昨天18:48
(月月 /译)肠道细菌能影响人类健康,如今已算不上新鲜事。许多人都知道这些微生物能够影响消化、过敏反应以及新陈代谢。上市的新书似乎都不约而同地详细列举出哪种饮食能让肠道细菌最为健康,大势已成,人们已司空见惯。
但这些微生物的影响可能更深入,深及人类大脑。肠道菌群的生态系统已为人所知,在世界各地,有越来越多的研究者正在探索这个微生物组(Microbiome)如何调节人类的想法和感觉。科学家们已经发现证据,这个总重一磅到三磅之间、包含着一千多种不同的细菌、由万亿个细胞共同形成的细菌集合物,在自闭症、焦虑症、抑郁症和其他的疾病中发挥着关键作用。
“对于肠道菌群和大脑之间的联系,人们突然兴趣激增”,加州大学洛杉矶分校的胃肠病学家埃默兰·迈耶(Emeran Mayer)如是说。在过去的五年里,迈耶一直从事这一领域的研究。
加些脆弱拟杆菌,就能改善自闭人们在关于自闭症的研究中取得了一些非常引人注目的成果。数十年来,医生、家长和研究人员已经注意到,大约四分之三的自闭症患者同时伴有某些胃肠功能异常,如消化问题、食物过敏或麸质过敏(gluten sensitivity)。这一发现促使科学家们检验肠道微生物与自闭症之间的潜在联系,近期的几项研究表明,自闭症患者的肠道菌群与对照组有显著差异。加州理工学院的微生物学家萨尔基斯·马兹曼尼亚(Sarkis Mazmanian)致力于研究肠道菌群中一种常见品种——脆弱拟杆菌(Bacteroides fragilis),人们已发现这种细菌在一些自闭症儿童体内数量较少。在两年前发表在《细胞》(Cell)杂志的一篇论文中,马兹曼尼亚和几个同事用取自人体的脆弱拟杆菌饲喂有类似于自闭症症状的小鼠,结果改变了小鼠体内的菌群组成,更重要的是,改善了它们的行为,使它们的焦虑程度降低,与其他小鼠的互动更多,表现出的重复性行为减少。
这些微生物具体如何与自闭症互相作用,微生物究竟是自闭症的一个触发器还是防护盾,这些都仍然迷雾重重。但是马兹曼尼亚和他的同事们已经确定了一个可能的关联物,即一种名为4-乙基苯酚硫酸盐(4-ethylphenylsulphate ,简称4EPS)的化学物质,该物质由肠道细菌产生。他们发现,有自闭症症状的小鼠,血液中4EPS水平比其他小鼠高出四十多倍。4EPS水平与大脑之间的关系尚不明确,但给小鼠注射了这一物质后,它们会出现类似自闭症的症状。
因其在肠道菌群方面的工作,马兹曼尼亚在2012年获得了麦克阿瑟奖。他将这一发现形容为对研究微生物如何在自闭症和其他神经发育障碍中起作用所取得的“潜在的突破性进展”。他表示,截至目前的研究结果表明,调整肠道细菌可能是治疗自闭症的一项可行的措施,至少对一部分病人来说是可行的。“也许我们可以扭转这一疾病”,他说,“如果除掉产生4EPS的源头,那么自闭症症状便会消失,这是我们在小鼠模型中发现的”。
加些双歧杆菌,就能减少焦虑科学家们也发现了肠道细菌影响焦虑和抑郁的一些证据。在加拿大安大略省汉密尔顿市,史蒂芬·柯林斯(Stephen Collins)是麦克马斯特大学的一位胃肠病学研究员,他发现乳杆菌属(lactobacillus)和双歧杆菌属(bifidobacterium)的两种细菌,能减少小鼠的焦虑样行为(科学家不称其为“焦虑”,因为你总不能去问一只老鼠它感受如何吧)。人类肠道中也有这两种细菌。在一项研究中,他和他的同事收集了有焦虑行为倾向的小鼠的肠道细菌,然后把这些细菌移植到了另外一批比较安静的小鼠体内,结果,原本安静的小鼠表现出了焦虑倾向。
总的来说,这两种微生物似乎是肠道——脑关联中的主要参与者。爱尔兰科克大学的神经科学家约翰·克莱恩(John Cryan)研究了它们对动物抑郁的影响。在2010年发表在《神经科学》(Neuroscience)杂志上的一篇论文中,他给予了大鼠双歧杆菌或者抗抑郁药依地普仑(Lexapro),然后将大鼠置于一系列应激环境中,其中一项实验是测量它们在一个没有任何出口的装满水的水槽中能持续游动多长时间(大鼠们在不长时间后就会被救出,以防溺死)。结果发现,这两者都有助于增加大鼠的耐力,并减少与压力相关的荷尔蒙分泌水平。在另一项实验中,他使用了乳杆菌,并得到了相似的结果。克莱恩正在进行一项以人为被试的研究(测试被试反应时所用的方法不包括强迫游泳实验)。
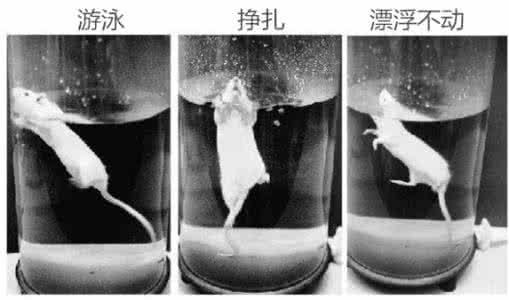
强迫游泳实验常被用于测试啮齿类动物的状态。比较抑郁的动物会很快放弃游泳,漂浮不动。而比较心怀期望的动物则能坚持游泳较长时间。图片来源:slideshare.net
到目前为止,大多数以菌群为基础的脑研究都是以老鼠为实验对象进行的,但是也已经有了一些以人为对象的研究。例如,柯林斯在去年将从焦虑症患者体内提取到的肠道细菌移植给了“无菌”小鼠——这些小鼠被专门仔细地饲养长大,它们的肠道中原本没有携带任何细菌。移植后,这些小鼠也表现得更为焦虑。
吃点益生元,就能降低压力还有一项研究,其对象是整个人体,而非仅仅是在人体寄生的细菌。牛津大学的神经生物学家菲尔·伯内特(Phil Burnet)发表在2015年5月的《精神病药理学》(Psychopharmacology)杂志上的一篇论文,研究了为肠道细菌提供支持的碳水化合物——益生元(prebiotic),是否能影响45名健康志愿者的压力水平。在实验中,部分受试者每天服下5.5克名为低聚半乳糖(galactooligosaccharide ,简称GOS)的粉状碳水化合物,而其他受试者服下的是安慰剂。在之前的大鼠实验中,这些研究者们已证实GOS能促进乳杆菌和双歧杆菌的生长,而肠道中乳杆菌和双歧杆菌数量多的大鼠,其体内影响焦虑的几种神经递质水平也更高,包括一种名为脑源性神经营养因子(BDNF)的神经递质。
在这个实验中,服用了GOS的受试者体内皮质醇的水平更低,那是一种关键的应激激素。当测试中,单词在屏幕上快速闪回时,服用了GOS的受试者更专注于积极的信息,对消极信息的关注则较少。这项测试常用于测量焦虑和抑郁水平,因为焦虑症和抑郁症患者往往非常关注威胁性的或消极的刺激。伯内特和他的同事们注意到,这个结果与受试者服用抗抑郁或抗焦虑药物得到的结果相似。
加州大学洛杉矶分校的研究者迈耶所做的人体研究可能是最为人所知的。他招募了25名健康的女性作为受试者,在四周时间里,受试者中的12人每天服用两次市售的酸奶,每次一杯。其余人则未曾服用。酸奶是一种益生菌,也就是说它含有活的细菌,在这个实验中用的酸奶含有四个属种的细菌,即双歧杆菌、链球菌(streptococcus)、乳球菌(lactococcus)和乳杆菌。在实验开始前和开始后,受试者都接受了脑部扫描来测量她们对一串面部表情图像的反应,包括愉悦、悲伤、气愤等。
出乎迈耶的意料,两组受试者在测试中的表现存在显著差异,服用酸奶的受试者对图像的反应比对照组更平静,该结果于2013年发表在《胃肠病学》(Gastroenterology)杂志上。“对比是明显的”,迈耶说。“我们完全没有料到这点。每天服用两次酸奶,持续几周就可以对你的大脑起一些作用。”他认为酸奶中的细菌改变了受试者肠道微生物的组成,从而导致产生了改变脑化学的物质。
肠道细菌,也许是下一代精神药物肠道菌群如何改变了大脑尚不明确。大多数研究者都认为这些微生物可能通过多重机制来影响大脑。科学家们已经发现肠道细菌能产生神经递质,如5-羟色胺、多巴胺和γ-氨基丁酸。这些神经递质在人的情绪方面发挥着关键作用(许多抗抑郁药物都是通过增加这些化合物的水平而发挥作用)。某些细菌还会影响人体对这些化合物的代谢,从而有效地调节它们在血液和脑中的水平。肠道细菌还可能产生其他的神经活性物质,包括一种叫做丁酸盐(butyrate)的物质,这种物质已被认为与减轻焦虑和抑郁有关。克莱恩和其他人的工作还表明,有些微生物能激活肠道和脑交联的主要途径——迷走神经。此外,肠道菌群与免疫系统息息相关,而免疫系统自身可以影响情绪和行为。
从进化论的视角来看,人体寄生细菌和脑的这种交互作用也可以解释。毕竟,细菌已在人体内居住了数百万年。克莱恩表示,随着时间推移,至少有一部分微生物已经发展出了基于自身目的而塑造宿主行为的方式。改变情绪是细菌一项可能的生存策略,他认为,“心情愉悦的人在社交中更为活跃。他们越热衷于社交,细菌获得交换和扩散的机会就越大。”
科学家们仍然在研究肠-脑细菌网络如何运作,克莱恩认为这可以用来治疗精神方面的疾病。“这些细菌最终可以像现在的百忧解或安定那样使用”,他说。因为这些微生物有长久地改变我们大脑的经验,它们可能比我们现在使用的药理学方式更加精确,更加敏感,这意味着副作用更小。“我认为这些微生物将在我们如何治疗这些疾病上发挥切实的作用”,克莱恩说,“这是一种全新的调节大脑功能的方式。” (编辑:游识猷) 爱华网
爱华网


