雅安市2015—2016学年下期期末检测高中二年级
化 学 试 题
请你在做题之前仔细阅读下列说明:
1.本试卷分选择题和非选择题两部分,第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。 2. 考试时间:90分钟;满分100分。
3. 答题前,考生务必将自己的姓名,准考证号填写清楚,并认真核对条形码上的准考证号,在规定的位置贴好条形码。
4.回答第Ⅰ卷(选择题)时,必须使用2B铅笔填涂;第Ⅱ卷(非选择题)必须使用0.5毫米黑色墨水签字笔书写、笔迹清楚。按照题号顺序在各题的答题区域内作答,超出答题区域的答案无效,在草稿纸上、试卷上答题无效。
5.保持卡面清洁,不要折叠、不要弄皱,禁用涂改液,涂改胶条。
第Ⅰ卷(选择题 共50分)
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Cr-52 Fe-56 选择题(共20个小题,每小题只有一个选项符合题目要求。1-10小题,每小题2分;
11-20小题,每小题3分;共50分。)
1.下列物质属于非电解质的是
A. 稀硫酸 A.NH4Cl
B.Cu
C.SO2 C.Na2CO3
D.NaOH D.Na2SO4 D.硅太阳能电池
2.室温下,0.1mol·L-1下列溶液的pH最大的是
B.NaHCO3
3.下列设备工作时,将化学能转化为电能的是
A.锂离子电池
B.太阳能热水器
C.天然气燃气灶
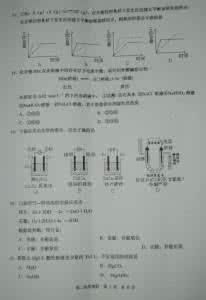
4.下列金属防腐的措施中,使用外加电流阴极保护法的是
A.水中的钢闸门连接电源的负极 B.金属护拦表面涂漆 C.汽车底盘喷涂高分子膜 D.地下钢管连接镁块
5.下列有机分子结构中,肯定既有σ键也有π键的是
A.C2H4
B.C2H5OH
C.C6H6 D.C3H8
6.分子式为C8H8的芳香烃,能使酸性KMnO4溶液褪色,也能跟溴水反应。该芳香烃与H2
在一定条件下完全加成,其生成物的一氯代物种数是 A.5种 液是 A.酸性
B.碱性
C.中性
D.无法判断
8.欲除去下列物质中混入的少量杂质(括号内物质为杂质),不能达到目的的是
A.乙酸乙酯(乙酸):加饱和Na2CO3溶液,充分振荡静置后,分液 B.乙醇(水):加入新制生石灰,蒸馏
C.溴苯(溴):加入稀NaOH溶液,充分振荡静置后,分液 D.乙酸(乙醇):加入金属钠,蒸馏 9.下列有关实验的叙述中,合理的是
A.用25mL碱式滴定管准确量取22.00 mL KMnO4溶液 B.用广泛pH试纸测出某盐酸的pH为3.2
C.使用pH试纸测定溶液pH时先润湿,则测得溶液的pH都偏小
D.实验室配制FeCl3溶液:先将FeCl3溶解在盐酸中,再加水稀释到所需要的浓度 10.把下列溶液加水稀释,溶液中每种离子的浓度都不会增加的是
A.H2SO4溶液 系正确的是
A.c(NH+ 4)>c(Cl-)>c(OH-)>c(H+) C.c(Cl-)>c(NH+ 4)>c(H+)>c(OH
-)
+)
B.6种 C.7种 D.8种
7.某温度时水的离子积为1×10-12,若该温度下某溶液中的H+ 浓度为1×10-7 mol·L-1,则该溶
B.Na2SO4溶液 C.Na2CO3溶液 D.FeCl3溶液
11.常温下,将pH=3的盐酸和pH=11的氨水等体积混合,完全反应后,溶液中离子浓度关
B.c(NH+ 4)>c(Cl-)>c(H+)>c(OH-) D.c(Cl-)>c(NH+ 4)>c(OH-)>c(H
12.已知常温下,KSP(AgCl)=1.8×10-10,KSP(AgI)=8.3×10-17,下列叙述中,正确的是 A.常温下,AgCl在饱和NaCl溶液中的KSP比在纯水中的KSP小 B.向AgCl的悬浊液中加入0.01mol·L-1KI溶液,沉淀由白色转化为黄色
C.将0.001mol·L-1的AgNO3溶液滴入KCl和KI的混合溶液中,一定先产生AgI沉淀 D.向AgCl的饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Ag+)=c(Cl-) 13.某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作
原理如图,下列说法正确的是 A.a为O2,b为CH4 B.CO2- 3向正极移动 C.此电池在常温时也能工作
D.正极电极反应式为2CO2+O2+4e-=2CO2- 3 14.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.pH=0的无色溶液:Al3+、Cu2+、SO2- 4、Cl-
B.使酚酞试液变红的溶液:Na+、Ca2+、HCO- 3、NO- 3
+-13-1+2+﹣18. 一定温度下,水中存在H2O?H+OH △H>0的平衡,下列叙述一定正确的是
A.向水中滴入少量稀盐酸,平衡逆向移动,Kw减小 B.将水加热,Kw增大,pH减小
C.向水中加入少量CH3COONa固体,平衡逆向移动,c(H+)降低 D.向水中加入少量Na2SO4固体,平衡不移动,c(H+)一定为10-7 mol·L-1
19.山梨酸(CH3-CH=CH-CH=CH-COOH)是一种常用的食品防腐剂。下列关于山梨酸性质的
叙述中,不正确的是 A.可与钠反应 B.可与碳酸钠溶液反应
C.可与溴的四氯化碳溶液发生取代反应 D.可生成高分子化合物
20.欲使醋酸溶液中的CH3COO-浓度增大,电离平衡向电离方向移动,且不放出气体,可向
醋酸溶液中加入少量固体 A.NaOH
B.NaHCO3
C.CH3COONa
D.Na
第Ⅱ卷(非选择题 共50分)
21(本题共9分).如图所示是某实验小组电解氯化钠溶液(含酚酞)的装置。有毒气体收集
22(本题共9分).某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池(如图
所示),得到的实验数据如下表所示:
爱华网www.aIhUaU.com网友整理上传,为您提供最全的知识大全,期待您的分享,转载请注明出处。 爱华网
爱华网



