依据氧化还原反应的电子守恒,可以计算化学反应中某物质的化合价、溶液中溶质的浓度、反应中各物质的比值、电化学中求某元素的相对原子质量、溶液的pH值等。这部分内容是高考中的常规考点,在各种题型中都可以出现。
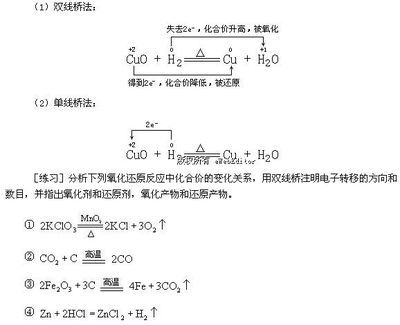
解题方法:氧化剂得到电子化合价降低转变为还原产物,还原剂失去电子化合价升高转变为氧化产物。在同一个氧化还原反应中得失电子数相等,即化合价升高总价数等于化合价降低总价数。
一、例题分析
【例题1】(NH4)2SO4在强热条件下分解,生成NH3、SO2、N2、H2O,反应中生成的氧化产物和还原产物的物质的量之比为
A. 1 : 3 B. 2 : 3 C. 1 : 1 D. 4 : 3
解析:(NH4)2SO4在强热条件下分解,氧化产物为N2,还原产物为SO2,依据化合价升降相等原则有3×2↑×x = 2↓×y,故有x : y = 1 : 3
答案:A
【例题2】R2O8n-在一定条件下可把Mn2+氧化为MnO4-,若反应中R2O8n-变为RO42-,又知反应中氧化剂与还原剂物质的量之比为5:2,则n值为:
A. 4 B. 3 C. 2 D. 1
解析:依题意有5R2O8n- + 2Mn2+ === 2MnO4- + 10RO42-,设R2O8n-中R的化合价为x,依据化合价升降相等原则有5×2×↓(x-6) = 2×↑(7-2),解得x = 7,因此有
2×7 + 8×(-2) = -n,解得n = 2.
答案:C
【例题3】(NH4)2PtCl6在强热条件下分解,生成N2、HCl、NH4Cl、Pt反应中氧化产物与还原产物的物质的量之比为
A. 1 : 2 B. 1 : 3 C. 2 : 3 D. 3 : 2
解析:(NH4)2PtCl6在强热条件下分解,氧化产物为N2,还原产物为Pt,依据化合价升降相等原则有3×2↑×x = 4↓×y,故有x : y = 2 : 3
答案:C
【例题4】Cl2与NaOH(70℃)的溶液中,能同时发生两个自身氧化还原反应,完全反应后,测得溶液中NaClO、NaClO3之比4 : 1,则溶液中NaCl和NaClO的物质的量之比为
A. 11:2 B. 1:1 C. 9:4 D. 5:1
解析:Cl2中氯元素的化合价为0价,而在NaClO、NaClO3中氯元素的化合价分别为+1、+5价,设NaCl和NaClO的物质的量分别为x和y,依据化合价升降相等原则有1↓×x = 1↑×y + 5↑××y,故有x : y = 9 : 4
答案:C
【例题5】含n克HNO3的稀溶液恰好与m克Fe完全反应,若HNO3只被还原为NO,则n : m可能是①5 : 1、②9 : 2、③3 : 1、④2 : 1、⑤4 : 1
A. ②③⑤ B. ①③④ C. ②③④ D. ①③
解析:当Fe恰好完全转变为+2价时,3Fe + 8HNO3 === 3Fe(NO3)2 + 2NO↑+ 4H2O,有 = 解得:n : m = 3 : 1
当Fe恰好完全转变为+3价时,Fe + 4HNO3 === Fe(NO3)3 + NO↑+ 2H2O,有
= 解得:n : m = 9 : 2
结合选项分析n : m的取值范围在4.5至3之间。
答案:A
【例题6】Zn与HNO3反应,Zn和被还原的HNO3的物质的量之比为4 : 1则HNO3的还原产物可能为
A. NO2 B. NO C. N2O D. NH4NO3
解析:设还原产物中氮元素的化合价为x,依据化合价升降相等原则有
4×2↑=1↓×(5-x) 解得:x = -3
答案:D
【例题7】将Mg和 Cu的合金2.64克,投入适量的稀HNO3中恰好反应,固体全部溶解时,收集的还原产物为NO,体积为0.896L(SPT),向反应后的溶液中加入2mol/L NaOH溶液60mL时,金属离子恰好完全沉淀,则形成沉淀的质量为
A. 4.32克 B. 4.68克 C. 5.36克 D. 6.38克
解析:依据在同一个氧化还原反应中得失电子数相等原则,解得Mg和 Cu共失去
n(e-) = ×3 = 0.12 mol,由电荷守恒知Mg和Cu共需要结合0.12 mol OH-,故形成沉淀的质量m = 2.64g + 0.12 mol×17g/mol = 4.68g
答案:B
【例题8】取x克Mg和 Cu的合金完全溶于浓HNO3中,反应过程中HNO3被还原只产生8960mL NO2和672mL N2O4气体(SPT),向反应后的溶液中加入足量的NaOH溶液,形成沉淀质量为17.02克,则X的值为
A. 8.64克 B. 9.20克 C. 9.00克 D. 9.44克
解析:依据在同一个氧化还原反应中得失电子数相等原则,解得Mg和 Cu共失去
n(e-) = ×1 = 0.46 mol,由电荷守恒知Mg和 Cu共需要结合0.46 mol OH-,因此有17.02g = x + 0.46 mol×17g/mol ,解得x = 9.20g
答案:B
【例题9】将14克Ag和Cu的合金与一定浓度的HNO3反应,全部溶解后,产生的气体再通入1.12L(SPT)O2,恰好完全吸收,求合金中各成分的含量?
解析:Ag和Cu失去电子的总数等于O2得到电子的总数,依题意有
解得n(Ag)= 0.1mol n(Cu)=0.05mol
w(Ag) = ×100% = 77.14%
w(Cu) = 1-77.14% = 22.86%

答案:合金中w(Ag)为77.14%,w(Cu)为 22.86%。
【例题10】将51.2 g Cu 完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、 N2O4 、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L的NaOH溶液完全吸收,生成NaNO3和NaNO2的混合溶液,其中生成的NaNO3的物质的量为
(已知NO+NO2+2NaOH === 2NaNO2+H2O,2NO2+2NaOH === NaNO3 +NaNO2 +H2O )
A. 0.2 mol B. 0.4 mol C. 0.6 mol D. 0.8 mol
解析:51.2 g Cu即为0.8 mol Cu,失去的电子等于NaNO2 生成时得到的电子,则NaNO2 为0.8 mol,由Na+守恒知:n(Na+) = n(NaNO2) + n(NaNO3),得NaNO3为0.2 mol。
答案:A
二、链接高考
【例题11】(2013·上海化学·18)汽车剧烈碰撞时,安全气囊中发生反应10NaN3 + 2KNO3 → K2O + 5Na2O + 16N2↑。若氧化物比还原物多1.75mol,则下列判断正确的是
A. 生成40.0LN2(标准状况) B. 有0.250molKNO3被氧化
C. 转移电子的物质的量为1.25mol D. 被氧化的N原子的物质的量为3.75mol
解析:根据反应方程式可知,每当生成16molN2,则氧化物比还原物多14mol。转移电子的物质的量为10mol,被氧化的N原子的物质的量为30mol,有2mol KNO3被还原,现氧化物比还原物多1.7mol,则生成2molN2,转移电子的物质的量为1.25mol,被氧化的N原子的物质的量为3.75mol,因此,C、D正确。
答案:C、D
考点定位:本题考查氧化还原反应计算
【例题12】(2013·上海化学·22)一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO12.0g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则V可能为
A. 9.0L B. 13.5L C. 15.7L D. 16.8L
答案:A
解析:若混合物全是CuS,其物质的量为12/80=0.15mol,转移电子数:0.15×(6+2)=1.2mol。两者体积相等,设NO xmol,NO2 xmol,3x+x1=1.2,计算的x=0.3。气体体积V=0.6×22.4=13.44L;若混合物全是Cu2S,其物质的量为0.075mol,转移电子数:0.075×10=0.75mol,设NO xmol,NO2 xmol,3x+x1=0.75,计算得x=0.1875,气体体积0.375×22.4=8.4L,因此选A。
考点定位:本题考查氧化还原反应计算(极限法)
三、跟踪练习
【练习1】9.8g镁、铝混合物溶解在一定量的热浓硝酸中,当金属完全溶解后收集到标准状况下8.96L NO2和2.24L N2O4气体,向反应的溶液中加入足量的氨水,则生成的沉淀有
A. 18克 B. 20克 C. 22克 D. 24克
解析:依据在同一个氧化还原反应中得失电子数相等原则,解得Mg和 Al共失去
n(e-)=×1 + ×2 = 0.6 mol。由电荷守恒知Mg和 Al共需要结合0.6 mol OH-,故形成沉淀的质量m = 9.8g + 0.6 mol×17g/mol = 20g
答案:B
【练习2】将11.2g的Mg和Cu的混合物完全溶解于足量的硝酸中,收集反应产生的气体X,再向所得溶液中加入适量的NaOH溶液,产生21.4g沉淀,根据题意推断气体X的成分可能是
A. 0.3mol NO2和0.3mol NO B. 0.2mol NO2和0.1mol N2O4
C. 0.1mol NO、0.2mol NO2和0.05mol N2O4 D. 0.6mol NO
解析:根据Mg、Cu的变化:Mg~Mg2+~2OH-~Mg(OH)2~2e-、Cu~Cu2+~2OH-~Cu(OH)2~2e-知增加的质量为OH-的质量,转移电子的物质的量与OH-的物质的量相等,则有n(OH-)=21.4g-11.2g/17g·mol-1 =0.6 mol,故反应转移的电子的物质的量也为0.6 mol。选项A转移电子的物质的量为0.3mol×1+ 0.3mol×3 = 1.2 mol,不正确;选项B转移电子的物质的量为0.2mol×1+ 0.1mol×2 = 0.4 mol,不正确;选项C转移电子的物质的量为0.1mol×3+ 0.2mol×1+ 0.05mol×2 = 0.6 mol,正确;选项D转移电子的物质的量为0.6mol×3=1.8 mol,不正确.
答案:C
 爱华网
爱华网