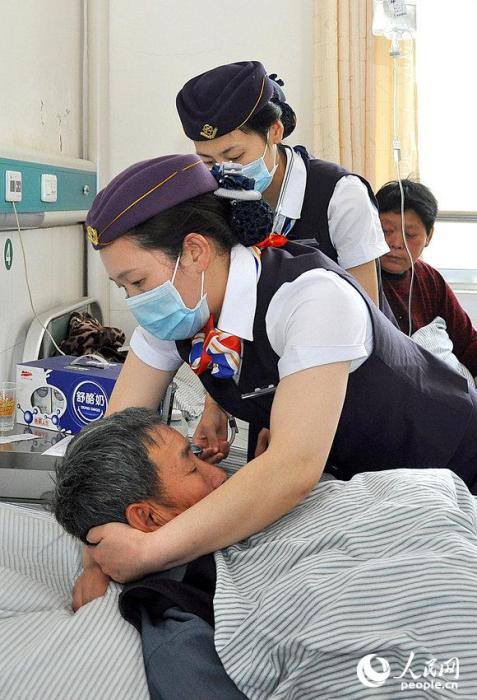
若限定溶液为无色溶液,则Cu2+、Fe3+、MnO4-、Co2+、Cr2O72-、CrO42-、Cr3+等有色离子不能存在。 (马上点标题下蓝字'初中化学'关注可获取更多学习方法、干货!)
在强酸性溶液中,OH-及弱酸根离子(比如CO32-、SO32-、S2-、CH3COO-等)均不能大量存在;
在强碱性溶液中,H+及弱碱阳离子(如NH4+、Al3+、Mg2+、Fe3+、等)均不能大量存在,多元弱酸的酸式酸根离子(如HCO3-、HSO3-、HS-、H2PO4-等)在强酸性和强碱性溶液中均不能大量存在。
①AlO2-与HCO3-不能大量共存,发生反应的方程式为AlO2-+ HCO3-+H2O==Al(OH)3↓+CO32-;
②“NO3-+H+”组合具有强氧化性,能与S2-、Fe2+、I-等发生发应,而这种组合常常较为隐蔽,不易被察觉;
③NH4+与CH3COO-,Mg2+与HCO3-等组合中,虽然两种离子都能水解且相互促进,但总的水解程度仍很小,他们在溶液中可以大量共存,但加热时不能大量共存。
能相互反应的离子显然不能大量共存。
①复分解反应,如Ba2+和SO42- 、OH-和NH4+、H+和CH3COO-、
②氧化还原反应,如Fe3+与I-
③相互促进的水解反应,如Al3+和HCO3-、Al3+和AlO2-等。
④生成配合物的反应,如Fe3+和SCN-等。
Tips:
大家在化学学习过程中还有哪方面知识学起来比较吃力,欢迎给化学姐留言,化学姐会尽力帮助大家。
百度搜索“爱华网”,专业资料,生活学习,尽在爱华网!
 爱华网
爱华网