虽然体系的内能和焓的绝对值目前还无法知道,但是在一定条件下我们可以从体系和环境间热量的传递来衡量体系的内能与焓的变化值。
焓_热焓 -基本内容
热焓及焓。它是表示物质系统能量的一个状态函数,通常用H来表示,其数值上等于系统的内能U加上压强P和体积V的乘积,即H=U+PV。
焓是热力学的基本概念之一。总的来说,封闭体系不做非体积功时的过程,内能变化可以通过测定恒容热效应来求,焓变可以通过测恒压热效应求得。
焓:H=U+PV,这里要说明一下,焓在这里无明确的物理意义,可以理解为,为了表达方便,专门设为一个符号,H即U+PV,之所以要提出焓这一物理量,是因为U+PV经常会用到,所以专门用一个符号来代替它。
由于我们不能确定体系内能的绝对值,所以也不能确定焓的绝对值。焓是状态函数,具有能量的量纲,但没有确切的物理意义,它的定义是由上式所规定下来的,不能把它误解为是“体系中含的热量”。我们所以要定义出一个新函数H,完全是因为它在实用中很重要,有了这个函数,在处理热化学的问题时就方便得多。
虽然体系的内能和焓的绝对值目前还无法知道,但是在一定条件下我们可以从体系和环境间热量的传递来衡量体系的内能与焓的变化值。在没有其它功的条件下,体系在等容过程中所吸收的热量全部用以增加内能,体系在等压过程中所吸收的热量,全部用于使焓增加。由于一般的化学反应大都是在等压下进行的,所以焓更有实用价值。
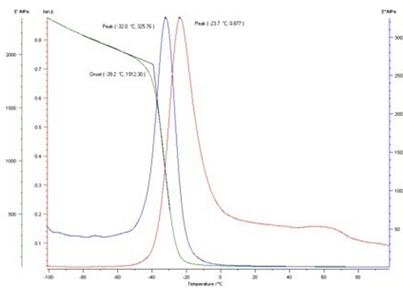
焓_热焓 -其他信息
SO3(g)+H2O(l)==H2SO4(l);ΔH= -130.3 kJ/mol
表示每生成1 mol H2SO4 放出 130.3 kJ 的热。
严格的标准热化学方程式格式: H2(g)+1/2O2(g)==H2O(l) ΔrHθm=-286kJ・mol-1(θ表示标准态,r表示反应,m表示1mol反应.含义为标准态下进行一摩尔反应的焓变)
我们设想在同一温度下发生同上的1mol反应:2H2(g)+O2(g)=2H2O(g),但不是在等温等容条件下,而是在等温等压条件下,或者说发生的不是等温等容反应,而使等温等压反应,若反应发生时同样没有做其他功,反应的热效应多大?这种热效应的符号通常用Qp表示,下标p表明等压,成为等压热效应。
Qp=△U+p△V=△U+RT∑vB(g)
式中△U≡U终态-U始态≡U反应产物-U反应物,式中∑vB(g)=△n(g)/mol,即发生1mol反应,产物气体分子总数与反应物气体分子总数之差。由该式可见,对于一个具体的化学反应,等压热效应与等容热效应是否相等,取决于反应前后气体分子总数是否发生变化,若总数不变,系统与环境之间不会发生功交换,于是,Qp=QV;若总数减小,对于放热反应
 爱华网
爱华网



