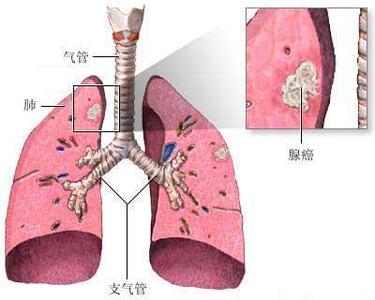
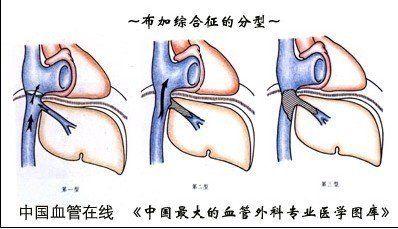
肝肺综合征(hepatopulmonary syndrome,HPS)是在慢性肝病和/或门脉高压的基础上出现肺内血管异常扩张,气体交换障碍,动脉血氧合作用异常导致的低氧血症及一系列病理生理变化和临床表现,临床特征在排除原发心肺疾患后的三联征―基础肝脏病、肺内血管扩张和动脉血氧合功能障碍。
肝肺综合症_肝肺综合征 -病因及发病率
肝肺综合征引发低氧血症的肝病病因:各种急、慢性肝病均可伴有肺血管异常和动脉低氧血症,最主要的是慢性肝病导致的肝硬化病人,特别是隐源性肝硬化、酒精性肝硬化、肝炎肝硬化及原发性胆汁性肝硬化。门静脉高压可能是肝肺综合征的主要发病因素,并未发现其与肝硬化严重程度具有相关性。研究认为HPS的发生发展是多种因素作用的结果,不能单纯用门脉高压或肝功能不全来解释。本病的发病率各家报道不一,各种慢性肝病发病率约5%~29% 。而肝硬化发生率较高。
肝肺综合症_肝肺综合征 -发病机理
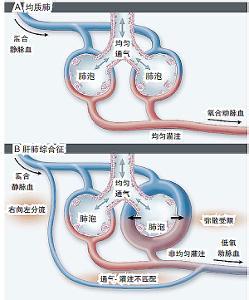
肝肺综合征HPS所致低氧血症最主要原因是肺通气/血流比例失调。HPS患者动脉低氧血症的确切发生机制仍不明确。Krowka等认为主要因为肺内血管扩张和分流的形成,加之缺氧性肺血管收缩受损和高动力循环的存在,而导致动脉低氧血症的发生。
1 、肺内分流的产生 HPS时由于肝脏功能严重受损,肠源性肺血管扩张物质不能被肝细胞灭活造成扩血管物质增多,如胰高血糖素、血管活性肠肽、前列腺素、血管紧张素-2、γ-氨酪酸、5-羟色胺等;或者为肺内皮局部对肠源性扩血管物质敏感性增加及肝功能障碍时,非肠源性肺血管扩张物质增多,如心房利钠肽、P物质、肿瘤坏死因子、血小板活化因子等。
2、 一氧化氮(NO)在HPS发病机制中的作用 HPS时肺内毛细血管扩张的原因中,一氧化氮(NO)在HPS发病机制中的作用成为研究热点。HPS时肺内NO生成增多,NO在肝硬化的高动力循环状态中起重要作用。Cremona观察到HPS患者呼出气体中NO含量是正常人的3倍,肝移植术后3月患者呼出气体中NO含量又恢复正常。HPS患者使用一氧化氮合酶(NOS)抑制剂亚甲蓝,患者的低氧血症可能得到迅速纠正。肺内NOS有两种:诱导型(iNOS)和内皮型(eNOS),Fallon等研究表明HPS肺组织和肺血管多为eNOS活性增强,iNOS活性无明显变化,说明肺内NO生成增多是肺内eNOS活性增强结果。同时,eNOS活性增强所致低氧血症、过度通气、A-aPO2增加、对新福林反应降低,些改变都可被NOS抑制剂所逆转。HPS时肺内eNOS合成增多的原因,与血浆内的内皮素-1(ET-1)、水平增加,及肺内eNOS的合成增多有关。HPS患者体内代谢产物的蓄积也是eNOS合成增多的原因之一。Zhang 等研究发现是eNOS的表达和活性明显增强,使NO产生增多,同时指出eNOS的表达和活性、循环血中ET-1水平、肺内血管扩张和气体交换三者之间存在相关性,而iNOS的表达无明显变化。但Nunes等却发现iNOS表达增强,使NO产生增多,而引起血管扩张。Liu等研究认为ET-1对肺内eNOS和NO的调节是通过一种ET受体依赖机制发生的,认为在正常情况下,ET-1被血管内皮细胞产生后优先进入血管壁内,与血管平滑肌细胞上的ET受体结合,产生缩血管作用,仅有少量进入管腔内,与血管内皮细胞上的ET受体结合而刺激NO的产生,来拮抗平衡它的缩血管作用;但在HPS时,ET-1可被肝脏过量生成,并可能通过破损的小管紧密连接进入血循环,产生一种内分泌性扩血管作用,优先与肺脏血管内皮细胞上的ET受体结合,增加eNOS的表达和活性,NO产生增多,引起肺内血管扩张。血浆内的ET-1水平和肝脏功能损害的严重程度之间有密切关系,可反应肝硬化的程度。目前的共识是:肺血管内吞噬细胞的诱导NOS活性表达升高使肺内NO产生过多,导致HPS发生。
3 、肺通气/血流比例失调 其它原因是肺外分流、肺内动脉高压、间质性肺纤维化。通过肝硬化的门静脉,血液进入食管静脉至此前纵隔静脉到达肺静脉。将低氧的门静脉血与已氧合的肺静脉血相混合而导致动脉性低氧血症,可造成心输出量增加和外周阻力降低。门静脉和肺静脉分流的形成是肝硬化患者氧合能力下降的重要原因。
4 、间质性纤维化 肝-肺同受肝炎病毒损伤所致的与免疫反应有关间质性肺纤维性肺泡炎临床表现为:肝炎后肝硬化致肺受损;肺-动脉瘘;肺动脉高压;肺纤维化;肺间质水肿;间质性肺炎;盘状肺不张。
肝肺综合症_肝肺综合征 -诊断
目前HPS的诊断还没有统一标准。诊断应以临床表现为基础,加以肺血管扩张的影像学证据进行诊断。有人认为肺基底部结节或网状结节阴影是肺内血管扩张的表现,但这种损害在尸体解剖中很难发现。X线检查的这种典型表现呈肺基底部的1.3~1.6mm中等大小结节状或网状结节状阴影表现,在慢性肝病患者中的发生率为5%~13.8%,而在HPS患者中可高达46%~100%。但此种表现有人认为并不具有特异性,也可存在于肺纤维化或肉芽肿性疾病,可通过肺功能测定,血管造影或CT检查等将其区分开。1.Rodriguer-Roisin等于1992年提出了HPS的诊断标准
(1)有慢性肝病存在,可无严重的肝功能不全。
(2)无心肺疾病,胸部X线检查正常或伴有肺基底部结节状阴影。
(3)肺气体交换异常,肺泡-动脉氧梯度增加(≥20kPa)。可有低氧血症。
(4)造影剂增强的二维超声心动图和(或)肺灌注扫描、肺血管造影证明存在肺血管扩张和(或)肺内血管短路。直立性缺氧、气短等临床表现是重要参考指标。
2.ChangSW等于1996年提出本病的诊断标准为
(2)低氧血症,卧位休息呼吸空气时的肺泡气-动脉血氧分压差[P(A-a)O2]≥2.67kPa或立位性缺氧。
(3)肺内血管扩张。
3.Krowka等于1997年认为当患者有门静脉高压、蜘蛛痣及杵状指时,强烈提示本病之诊断,需行相关检查以便确诊。诊断的标准为:
(1)99mTc-MAA扫描、造影剂增强的二维超声心动图、肺血管造影检查等证实存在肺内毛细血管扩张,
(2)存在慢性肝脏疾病和低氧血症PaO2<9.3kPa(70mmHg)。
国内高志等于1998年认为本病的诊断需根据患者有肝脾肿大、腹水、肝掌、蜘蛛痣、劳累性呼吸困难、平卧呼吸及直立性缺氧,胸片显示肺基底部的间质及血管纹理增多,可呈斑片状或结节状、网状结节状阴影,CT显示基底部肺血管扩张、肺血管支增多,血气分析不一定有严重低氧血症,但肺泡-动脉氧梯度增大≥20kPa,肺功能检查82%有弥散障碍等检查综合分析。此外还需行有关分流的检查,如99mTc-MAA扫描、造影剂增强的二维超声心动图、肺血管造影检查等,但后者不如前两者敏感,因为肺内小的血管扩张在造影时不一定有表现。Binay等认为肝硬化患者临床上无发绀、杵状指及蜘蛛痣,动脉血气分析、PaO2及肺功能测试均可正常,而气泡造影超声心动图检查阳性的患者,已出现肺血管扩张,被称为“亚临床型”肝肺综合征,需引起临床重视。
实验室检查:血气分析:低氧血症是肝肺综合征的基本病理生理改变,因此血气分析为诊断本病所必需,在没有原发心肺疾患的肝病患者如出现较明显的低氧血症则提示本病之诊断。主要表现为:动脉血氧分压(PaO2)<9.33kPa(70mmHg),肺泡-动脉血氧梯度增大(>4.53kPa或34mmHg),患者由于缺氧可致:如动脉血二氧化碳分压(PaO2)下降,pH值升高。目前认为PaO2下降是必备条件。但也有人认为肺泡-动脉血氧梯度增大或许更灵敏。
其他辅助检查:
1.肺功能测定可测定肺活量、最大通气量、功能残气量、肺总量、呼吸储备容积、R/T、1s用力呼气容积量、肺一氧化碳弥散量等。在无明显胸、在。
腹水的肝肺综合征患者虽然肺容量及呼气量可基本正常,但仍有较明显的弥散量改变,即使校正血红蛋白后仍明显异常。一般肝病发展到晚期均有肺功能紊乱,可表现为肺呼气量下降、呼吸道阻力增加、气体弥散功能受损等。在肺功能检查发现有呼气阻力增加时应做相应检查;如
 爱华网
爱华网