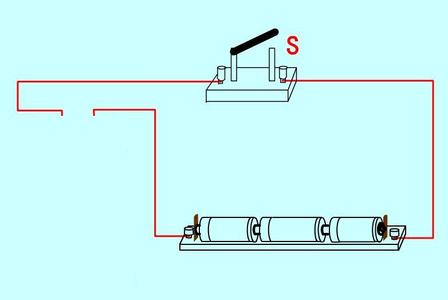
将化学能转变为电能的装置称为原电池。在原电池中,发生的化学反应是氧化还原反应。发生氧化反应的一极上有电子流出,做负极,失去电子的物质是还原剂。电子通过原电池的负极经导线流向正极,在正极上氧化剂得到电子,发生还原反应。原电池就是通过化学反应实现化学能向电能转化的。
原电池反应_原电池反应 -基本内容
1.了解原电池的组成
组成原电池有三个不可缺少的条件,这三个条件是:
(1)电极 由两块活泼性能不同的金属作为原电池的两个电极。活泼的金属是电池的负极,不活泼金属(或非金属导体)是电池的正极。
(2)电解质溶液 根据电解材料,可以选择酸、碱、盐溶液作为组成的电解质溶液。
(3)导线 用以连接两极,才能使浸入电解质溶液的两极形成闭合回路,组成正在工作的原电池。
2.理解原电池的工作原理
当把锌板和铜板平行放入盛有稀硫酸的烧杯里,用连有电流计的导线连接两极时,可以观察到三个重要的现象:锌片溶解,铜片上有气体逸出,导线中有电流通过。
此外,在食盐溶液加快生锈的过程中,也发生了原电池反应
透过这些现象,分析两极反应的实质,便可理解原电池是怎样把化学能转变为电能的原理。锌是活泼金属,容易失去电子变为进入溶液,锌电极发生的电极反应式是:
锌片 Zn-2e-=Zn2+ (氧化反应)
锌失去的电子沿导线经电流计流入铜片,溶液里的在铜电极上得到电子变为氢原子,进而结合为氢分子,铜电极发生的电极反应式是:
铜片 2H+2e-=H2↑ (还原反应)
由于在锌、铜两个电极上不断发生的氧化还原反应,使化学能转变为电能。锌片是给出电子的一极,是电池的负极,铜片是电子流入的一极,是电池的正极。电流的方向同电子流的方向相反,从正极铜流向负极锌。
在原电池内电解质溶液中,阴离子流向负极,阳离子流向正极
 爱华网
爱华网