化学键:由于粒子对电子吸引力大小的不同,使键电子偏向一方的共价键称为极性键,由一方提供成键电子的化学键称为配位键。极性键的两端极限是离子键和非极性键,离域键的两端极限是定域键和金属键。
化学键_化学键 -定义
化学键
化学键(chemical bond)是指分子或晶体内相邻原子(或离子)间强烈的相互作用。
2分类:金属键、离子键、共价键。
在水分子H2O中2个氢原子和1个氧原子通过化学键结合成水分子 。化学键有3种极限类型 ,即离子键、共价键和金属键。离子键是由阴阳离子的静电作用,例如氯和钠以离子键结合成NaCl。共价键是两个或几个原子通过共用电子对产生的吸引作用,典型的共价键是两个原子借吸引一对成键电子而形成的。例如,两个氢核同时吸引一对电子,形成稳定的氢分子。金属键则是金属阳离子和自由电子形成,可以看成是高度离域的共价键。定位于两个原子之间的化学键称为定域键。由多个原子共有电子形成的多中心键称为离域键。除此以外,还有过渡类型的化学键:由于粒子对电子吸引力大小的不同,使键电子偏向一方的共价键称为极性键,由一方提供成键电子的化学键称为配位键。极性键的两端极限是离子键和非极性键,离域键的两端极限是定域键和金属键。
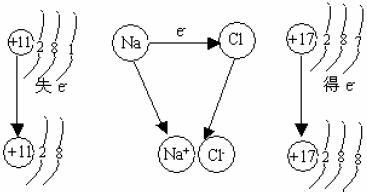
电子-模型图
化学键_化学键 -分类
图解说明各种化学键之间的联系
化学键有3种极限类型,即离子键、共价键和金属键。
1、离子键[1]是由正负离子之间通过静电引力吸引而形成的,正负离子为球形或者近似球形,电荷球形对称分布,那么离子键就可以在各个方向上发生静电作用,因此是没有方向性的。
2、一个离子可以同时与多个带相反电荷的离子互相吸引成键,虽然在离子晶体中,一个离子只能与几个带相反电荷的离子直接作用(如NaCl中Na+可以与6个Cl-直接作用),但是这是由于空间因素造成的。在距离较远的地方,同样有比较弱的作用存在,因此是没有饱和性的。
定位于两个原子之间的化学键称为定域键。由多个原子共有电子形成的多中心键称为离域键。除此以外,还有过渡类型的化学键:键电子偏向一方的共价键称为极性键,由一方提供成键电子的化学键称为配位键。极性键的两端极限是离子键和非极性键,离域键的两端极限是定域键和金属键。
化学键_化学键 -简史
化学键的概念是在总结长期实践经验的基础上建立和发展起来的,用来概括观察到的大量化学事实,特别是用来说明原子为何以一定的比例结合成具有确定几何形状的、相对稳定和相对独立的、性质与其组成原子完全不同的分子。开始时,人们在相互结合的两个原子之间画一根短线作为化学键的符号;电子发现以后,1916年G.N.路易斯提出通过填满电子稳定壳层形成离子和离子键或者通过两个原子共有一对电子形成共价键的概念,建立化学键的电子理论。
量子理论建立以后,1927年W.H.海特勒和F.W.伦敦通过氢分子的量子力学处理,说明了氢分子稳定存在的原因,原则上阐明了化学键的本质。通过以后许多人,特别是L.C.鲍林和R.S.马利肯的工作,化学键的理论解释已日趋完善。
化学键_化学键 -分类方法
碳分子中的化学键示意图
共价键有不同的分类方法。
(1) 按共用电子对的数目分,有单键(Cl―Cl)、双键(C=C)、叁键(C C)等。
(2) 按共用电子对是否偏移分类,有极性键(H―Cl)和非极性键(Cl―Cl)。
(3) 按提供电子对的方式分类,有正常的共价键和配位键(共用电子对由一方提供,另一方提供空轨道。如氨分子中的N―H键中有一个属于配位键)。
(4) 按电子云重叠方式分,有σ键(电子云沿键轴方向,以“头碰头”方式成键。如C―C。)和π键(电子云沿键轴两侧方向,以“肩并肩”方向成键。如C=C中键能较小的键。)等
2、旧理论:共价键形成的条件是原子中必须有成单电子,自旋方向必须相反,由于一个原子的一个成单电子只能与另一个成单电子配对,因此共价键有饱和性。如原子与Cl原子形成HCl后,不能再与另外一个Cl形成HCl2了。
3、新理论:共价键形成时,成键电子所在的原子轨道发生重叠并分裂,成键电子填入能量较低的轨道即成键轨道。如果还有其他的原子参与成键的话,其所提供的电子将会填入能量较高的反键轨道,形成的分子也将不稳定。 像HCL这样的共用电子对形成分子的化合物叫做共价化合物
化学键_化学键 -化学键和分子间的作用力
一、化学键:1,含义:分子或晶体内相邻原子(或离子)间强烈的相互作用。
2,类型,即离子键、共价键和金属键。
离子键是由异性电荷产生的吸引作用,例如氯和钠以离子键结合成NaCl。
(1),使阴、阳离子结合的静电作用
(2),成键微粒:阴、阳离子
(3),形成离子键:a活泼金属和活泼非金属
b部分盐(Nacl、NH4cl、BaCo3等)
c强碱(NaOH、KOH)
d活泼金属氧化物、过氧化物
(4),证明离子化合物:熔融状态下能导电
共价键是两个或几个原子通过共用电子
(1),共用电子对对数=元素化合价的绝对值
(2),有共价键的化合物不一定是共价化合物
对产生的吸引作用,典型的共价键是两个原子借吸引一对成键电子而形成的。例如,两个氢核同时吸引一对电子,形成稳定的氢分子。
(1),共价分子电子式的表示,P13
(2),共价分子结构式的表示
(3),共价分子球棍模型(H2O-折现型、NH3-三角锥形、CH4-正四面体)
(4),共价分子比例模型
补充:碳原子通常与其他原子以共价键结合
乙烷(C-C单键)
乙烯(C-C双键)
乙炔(C-C三键)
金属键则是使金属原子结合在一起的相互作用,可以看成是高度离域的共价键。
二、分子间作用力(即范德华力)
特点:a存在于共价化合物中
b化学键弱的多
c影响熔沸点和溶解性--对于组成和结构相似的分子,其范德华力一般随着相对分子质量的增大而增大。即熔沸点也增大(特例:HF、NH3、H2O)
 爱华网
爱华网



