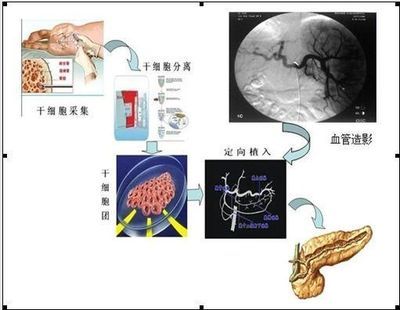
造血干细胞(hemopoieticstemcellHSC)是存在于造血组织中的一群原始造血细胞,它不是组织固定细胞,可存在于造血组织及血液中。造血干细胞在人胚胎2周时可出现于卵黄囊,妊娠5个月后,骨髓开始造血,出生后骨髓成为干细胞的主要来源。在造血组织中,所占比例甚少。现代医学中,造血干细胞在骨髓移植和疾病治疗方面有重要作用。
造血干细胞_造血干细胞 -简介
造血干细胞
干细胞是一种嗜碱性独核细胞,其大小约为8μm,呈圆形,胞核为圆形或肾形,胞核较大,具有2个核仁,染色质细质而分散,胞浆呈浅蓝色不带颗粒,在形态上与小淋巴细胞极其相似,但淋巴细胞体积较小,染色质浓染,核仁不明显且有细胞器。
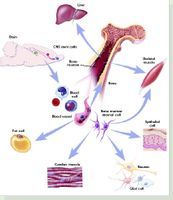
造血干细胞(Stemcell,SC)是指骨髓中的干细胞,它具有自我更新能力并能分化为各种血细胞前体细胞,最终生成各种血细胞成分,包括红细胞、白细胞和血小板,它们也可以分化成各种其他细胞。造血干细胞包括三级分化水平,即多能干细胞(pleuripotentstemcell),定向干细胞(Committedstemcell)及成熟的子代细胞。造血干细胞的两个重要特征是,可分化成所有类型的血细胞和高度的自我更新或自我复制能力。
造血干细胞的移植是治疗血液系统疾病、先天性遗传疾病以及多发性转移性肿瘤疾病的最有效方法。与骨髓移植和外周血干细胞移植相比,造血干细胞移植的长处在于无来源的限制,对HLA配型要求不高,不易受病毒或肿瘤的污染。并且捐献造血干细胞对捐献者的身体并无很大伤害。
造血干细胞_造血干细胞 -形成过程
哺乳动物的造血最早发生在卵黄囊,随后转移到胎肝,胚胎发育中期以后以及出生后,骨髓成为主要的造血场所,并为B细胞发育的中枢免疫器官。造血干细胞是存在于造血组织中的一群原始造血细胞,它不是组织固定细胞,可存在于造血组织及血液中。造血干细胞在人胚胎2周时可出现于卵黄囊,第4周开始转移至胚肝,妊娠5个月后,骨髓开始造血,出生后骨髓成为干细胞的主要来源。早期的造血干细胞是多能造血干细胞(pluripotenthematopoieticstemcell),具有自我更新和分化两种重要的潜能,多能造血干细胞最初分化为共同淋巴样祖细胞和共同髓样祖细胞等。在造血组织中,所占比例甚少,如在小鼠骨髓中105核细胞中的有10个,在脾中105有核细胞中只有0.2个。
造血干细胞_造血干细胞 -表面标志
由于造血组织中造血干细胞在形态学方面无法与其它单核细胞区别,而且数量极少,这为造血干细胞的分离纯化并对其功能分析和分化的研究造成极大困难。由于单克隆抗体技术的进步,流式细胞仪(FACS)的应用,以及对小鼠和人造血干细胞表面标志的研究,取得了很大进展,为造血细胞的分离纯化及鉴定创造了条件。
Thy-1与丝裂原(wheatgermagglutininWGA)
Visseer等发现小鼠骨髓中造血干细胞对WGA有高亲和性。利用这一特性,应用FACS自骨髓中分离造血干细胞应及核系Mac-1等谱系抗原与WGA反应性相结合,即可自骨髓中Lin-/WGA 细胞群中分离造血干细胞,也获得良好结果。
也有学者发现正常小鼠骨髓细胞中,也能表达低密度Thy-1抗原(Thy-11)。Lin-WGA 细胞群中,分离造血干细胞,可用于对造血细胞的功能分析。
干细胞抗原(stemcellantigen-1Sca-1)
有学者制备一种抗原前T细胞杂交瘤的单克隆抗体,用这种单抗检出的抗原分子称为干细胞抗原-1(Sca-1)。从骨髓的Thy-1Io、Lin-、Sca-1 细胞群中,可分离纯人造血干细胞。
原癌基因(c-kit)
造血干细胞与c-kit基因密切相关。C-kit可编码一种穿膜酪氨酸激酶受体分子。应用单克隆抗体证明此分子可存在于造血干细胞膜上,证明它的配体分子是造血干细胞因子(stemcellfactorSCF)。它是信号传导分子,对造血干细胞的分化具有重要作用。小鼠多能干细胞表面分子标志可视为Thy-1Io、WGA 、c-kit 、Lin-。
c-kit分子可高频率表达于多能干细胞表面,但骨髓中c-kit 细胞可分化为各种血细胞,而胸腺中c-kit细胞可分化为淋巴细胞,不能分化为髓系细胞,所以胸腺内c-kit 细胞,可能是淋巴样干细胞。
CD34
对人体造血干细胞表面标志的研究,是用单克隆抗体CD34证明的。CD34单克隆抗体检测的抗原即为CD34分子。自人骨髓细胞中应用FACS可分离纯化CD34 细胞群,如与造血因子共同体外培养可获得含有各种血细胞的混合集落,所以CD34 细胞为骨髓中造血干细胞,CD34抗原可视为骨髓造血细胞标志之一。
造血干细胞_造血干细胞 -分化
造血干细胞可分化为多能干细胞和单能干细胞。
多能干细胞
多能干细胞是由Till和McCulloch,应用脾集落形成细胞定量法,首先在小鼠体内证明的。给经射线照射的小鼠输入同系鼠骨髓细胞,在10-14天后在脾内形成可见的结节,它是由单一骨髓细胞发育分化而成的细胞集落,称之为脾集落形成单位(colonyformingunit-spleenCFU-S)。集落数与输入的细胞数成正比,它可分化发育为红细胞、粒细胞及巨核细胞。CFU-S长期以来用体内集落法进行检测。
Johnson和Metcalf等应用鼠胎肝细胞体外培养法,证明具有CFU-S性质的干细胞可在体外培养成功,在研究干细胞方法学上取得重大改进。
Haral等用小鼠骨髓细胞在甲基纤维素中加入红细胞生成素(erythropoietinEPO)及脾细胞培养上清,进行体外培养,可形成含有红细胞、巨核细胞以及巨噬细胞的集落(称为混合集落形成单位CFU-Mix)。小林登等在用人骨髓细胞亦报告CFU-Mix培养成功。即由多能干细胞可进一步分化为定向髓系多能干细胞及淋巴系干细胞。
单能干细胞
单能干细胞是一类具有向特定细胞系分化能力的干细胞,也称为祖细胞(progenitor)。如进行体内移植不能形成脾集落,但在一定造血因子的存在下,可在体外培养并形成细胞集落,称为体外培养集落形成单位(colonyformingunit-cultureCFU-C),因此它与多能干细胞不同,它可包括分化为红细胞的红系干细胞,可分化为粒细胞和单核细胞的粒、单核细胞干细胞系及血小板的巨核干细胞系。
1.红系干细胞应用骨髓细胞加甲基纤维素在大量EPO存在下,进行体外培养可产生大型红细胞集落,可含有1000个以上的细胞,形成如爆发火花样的集落,称此干细胞为爆式红细胞集落形成细胞(burstunit-erythoidBFU-E)。
2.粒细胞-单核细胞系干细胞此系细胞在功能上与BFU-E或CFU-E属同级干细胞。应用软琼脂法将骨髓细胞进行体外培养,在集落刺激因子(CFS)存在下,可产生粒细胞和单核细胞集落,称此集落形成细胞为体外培养集落形成细胞(colonyformingunti-cultureCFU-C)。将CFU-C进行体内移植不能产生脾集落,所以CFU-D不具有CFU-S的特性,仅具有前驱细胞和前驱单核细胞的特征。
3.巨核干细胞系亦称巨核细胞集落形成细胞(colonyformingunti-megakaryocyteCFU-M),Metcalf及其分泌的细胞因子和细胞外基质(extra-cellularmatrixECM)组成,因此对造血干细胞发育分化过程的体外研究,有很大局限性,它不一定能真实反映体内情况,分析实验结果时,必须注意这种局限性。
造血干细胞_造血干细胞 -与淋巴细胞的关系
造血干细胞与淋巴细胞
由于用脾集落法未能证明淋巴细胞的发生, 所以造血干细胞与淋巴细胞在发生学的关系,直到Wu等建立了放射诱导染色体标记技术后才逐步得到阐明。
Wu等用照射诱导小鼠骨髓干细胞染色体发生一定程度的畸变,做为标记,但又不影响其细胞分裂。将这种细胞输入另一照射小鼠体内后,可以重建其造血和免疫功能。
由于它们具有特殊的畸形染色体,因此在照射宿主体内,任何二种细胞只要它们有共同的标记染体,应表明它们是来自同一干细胞。由于在照射诱导条件下,骨髓细胞中分化程度不同的干细胞,可以产生不同类型的染色体畸变,所以通过核型分析就能检查不同细胞的共同前体细胞。
造血干细胞与淋巴细胞都是从供体骨髓中的多能干细胞分化而来,无论是髓系干细胞和淋巴细胞,都是来自共同的造血干细胞。
造血干细胞_造血干细胞 -主要作用
造血干细胞的应用
造血干细胞是血液成分之一,是生成各种血细胞的最起始细胞,又称造血多能干细胞,存在于骨髓、胚胎肝、外周血及脐带血中。它既具有高度自我更新能力,又具有进一步分化各系统祖细胞的能力。近代输血就利用这两种能力,对受血者用放射或大剂量化学药物使其免疫系统受抑再输入献血者的造血干细胞,让它在受血者骨髓内“定居”下来,分化增殖,这即是造血干细胞移植。造血干细胞移植包括骨髓移植(BMT),胎肝造血细胞移植,外周血干细胞(PBSC)移植及脐带血造血细胞移植。
BMT是临床最常用的造血干细胞移植。临床分为同基因BMT(SBMT)、异基因BMT(ALLO-BMT)及自身BMT(ABMT)三种类型。前两种主要用于肿瘤性血液病,遗传性血液病及某些代谢性疾病,而自身BMT多用于白血病和实体瘤患者。脐血可用于同基因或异基因移植,也可用于自身造血重建,凡符合BMT适应症的病均可用脐带血移植代替。
人胎肝造血细胞临床应用方式有两种,一种为胎肝细胞输注(FLCI),另一种是胎肝移植(FLT)。胎肝细胞用于临床由于取材方便,输注安全,不发生严重的移植物抗宿主病,故显示一定的前景。外周血肝细胞移植的临床应用报道有治疗急性白血病、慢性粒细胞性白血病及恶性肿瘤。与骨髓、胚胎肝的造血干细胞移植相比,外周血肝细胞移植的优点是造血及免疫功能重建早;放射线的敏感性低,受体内植入率高;自身外周血残存肿瘤细胞比骨髓少;采集方便、不需骨髓穿刺,易被接受。由于移植免疫学的进展,人类造血干细胞移植已进入一个新的发展阶段,它已成为细胞工程学中的一个重要组成部分。
造血干细胞_造血干细胞 -临床应用
生命科学是二十世纪发展最为迅猛的学科之一,已经成为自然科学中最引人注目的领域。1957年,美国华盛顿大学多纳尔・托玛斯发现正常人的骨髓移植到病人体内,可以治疗造血功能障碍。这一技术的发现,使多纳尔・托玛斯本人荣获了诺贝尔奖。这一技术很快得到全世界的认可,并已成为根治白血病等病的主要手段。造血干细胞移植技术的发现和应用为人类战胜疾病带来新的希望。
造血干细胞移植可治疗恶性血液病,部分恶性肿瘤,部分遗传性疾病等75种致死性疾病。包括急性白血病、慢性白血病、骨髓增生异常综合征、造血干细胞疾病、骨髓增殖性疾病、淋巴增殖性疾病、巨噬细胞疾病、遗传性代谢性疾病、组织细胞疾病、遗传性红细胞疾病、遗传性免疫系统疾病、遗传性血小板疾病、浆细胞疾病、地中海贫血、非血液系统恶性肿瘤、急性放射病等。因为造血干细胞移植技术,众多疑难疾病有了治愈的可能。
造血干细胞_造血干细胞 -采集
采集量标准
成年人(18~45岁)的骨髓量一般在3000克左右,大部存于骨髓腔。成人一例采集量为50―200ml造血细胞悬液,采集次数不超过2次。一般循环处理血量不少于10000ml。CD34+>2×106/kg、MNC>5×108/kg。每天检测CD34+量,在最高峰时间采集,对捐献者本身无不良影响。
胎盘造血干细胞采集方法
1.新生儿娩出后,在距新生儿脐部10厘米处用两把止血钳夹住脐带,再从两钳间剪断脐带后结扎,最好再用75%乙醇消毒脐带残端、脐带根部及其周围,新生儿抱走正常处理。
2.待胎盘娩出后,用医用手术缝线或其他适宜的材料结扎胎盘上婴儿端的脐带。
3.用0.9%生理盐水将胎盘脐带涮洗一到两次,以清除胎盘上的羊水及胎粪等污物,避免胎盘脐带与其他物品接触。
4.将采集好的胎盘脐带放入无菌一次性胎盘采集盒,盖好盒盖,并确认采集液没过胎盘。
采集渠道
一般造血干细胞来源于三个渠道:
1、骨髓造血干细胞。
2、外周造血干细胞。
3、脐带血造血干细胞。
中华骨髓库目前主要开展外周血造血干细胞采集。
三种来源及应用对比:
移植方式外周血造血干细胞骨髓造血干细胞脐带血造血干细胞成份较为单一的造血干细胞除造血干细胞外还有其他血液成份除造血干细胞外还有其他血液成份采集方法在上臂血管采集
不住院不麻醉,采集前注射动员剂无痛苦在髓骨上钻孔采集
需住院需麻醉不需注射动员剂有痛苦收集脐带血移植应用普遍较少只适用25KG下儿童成本低高很高采集及恢复时间2-4天半年--保存无需保存无需保存实体保存应用普遍较少很少
造血干细胞_造血干细胞 -储存
胎盘造血干细胞的储存流程
进行完胎盘采集后,在限定时限内将胎盘运送到干细胞库,由专业的技术人员进行胎盘造血干细胞的分离、提取、检测等技术流程,直到根据最终检测结果来确认所获得的干细胞是否具有长期保存的价值。
保存期限
国际上通用的干细胞保存技术是将获得的干细胞储存在-196℃深低温状态,医学研究与临床实践证明保存一百多年的细胞仍然具有活性,而干细胞已有几十年的保存历史,胎盘干细胞库在与客户签订的合同期限内对干细胞库中所保管的胎盘造血干细胞活性负责。
造血干细胞_造血干细胞 -对捐献者的影响
生理无损健康
人体血液中有多种血细胞,红细胞、白细胞、血小板等,它们都是有寿命的,多则120天,少则36小时,不断新陈代谢。它们均来自于一种始祖细胞,我们称它为造血干细胞。造血干细胞具有高度的自我更新、自我复制的能力,可分化生成各种血细胞。造血干细胞有很强的再生能力,失血或捐献造血干细胞后,可刺激骨髓加速造血,1-2周内,血液中各种成分可恢复到原来水平。
适龄、健康的志愿者捐献造血干细胞后,由于血细胞数量减少,会促使骨髓把储备的白细胞释放,并刺激骨髓造血功能,促使血细胞的生成,不会影响身体健康。人体的造血干细胞主要存留在长骨的骨髓腔和扁平骨的稀松骨质间的网眼内,这是一种红色的海绵状组织,被称为红骨髓。人出生时,红骨髓充满全身骨髓腔,随着年龄长大,脂肪细胞增多,相当部分红骨髓变成黄骨髓。此种变化是由于成人不需要全部骨髓参加造血,部分骨髓造血已经足够补充所需血液。当身体严重缺血时,部分黄骨髓又可以变成红骨髓而继续进行造血。
实践安全
中国大陆已经采集1700多例造血干细胞,这是无血缘关系的,有血缘关系的则更多;台湾已经采集800多例造血干细胞(大部分为骨髓)。国际上美国已经采集2万多例造血干细胞(大部分为骨髓);日本已经采集5500多例造血干细胞(全部是骨髓)。据多年的临床观察和国际上的报道,至今还没有因采集外周血造血干细胞引起对捐献者伤害的案例。在采集完成后,一些轻微疼痛感和不适将很快消失。动员剂安全
从外周血采集造血干细胞简单、省事,故中国捐献造血干细胞较多采用此种方法。但在正常生理条件下,外周血的造血干细胞数量少,不能满足移植的需要,如注射细胞动员剂,可使外周血造血干细胞增加20~30倍。目前使用的细胞动员剂是“粒一巨噬细胞集落刺激因子(GM--CSF)”,除能增加外周血造血干细胞的数量外,还有辅助心脏功能等作用。一般没有对人体健康的危害和副作用。
技术成熟
中华骨髓库有经专家委员会审定的移植医院和采集医院(中心),在这样的医院里采集造血干细胞如同采集成分血一样简单、安全。在整个采取过程中所用的器材都经过严格消毒,并一次性使用,确保了捐献者的安全。
 爱华网
爱华网