医药行业是一个产品导向性很强的行业,产品可以说是医药企业的命根子,多少药老板凭借一两个好产品“发家致富”或是 “咸鱼翻身”。因此,药老板们坐在一起谈论得最多的就是各家的产品。个个都想在成百上千的研发产品堆里挖到一个“聚宝盆”。
既然产品如此重要,筛选新产品的过程,也就是新产品立项自然就是很重要的事了,为此,在药企里,一般都是大老板亲自抓新产品立项。倘若单说挑选产品的能力,经过多年市场摸爬滚打的老板们,自然是当能不让。可是随着企业业务的发展,他们多半都把精力投入到更为紧急的营销和公关事务之中。而对于新产品立项这一重要工作,老板们一方面是不放心别人,紧抓不放;一方面又是事务缠身,力不从心,于是拍拍脑袋就决定了。这样就引发出很多新产品立项的问题:
常见的是“红眼病”,看到别人开发了一个好产品,口口声声:“不惜一切代价也要上这个项目!”。于是,不久之后,放眼望去,满市场都是这个品种。要不就是“暴饮暴食”,恨不得从头到脚各科室的药都想搞上几个品种,立项时是“多多益善”,到后期资金、人力严重吃紧,多数项目“搁浅”在临床阶段,严重“消化不良”。还有就是“急火攻心”, 看到有个“好苗子”,便“一见钟情”,不问清对方家底便草率行事,等到申报时才“如梦初醒”:不是尚在保护期,就是原料有问题!
将这些毛病归归类,可以归结为三个层面:战略层面、职能层面和操作层面。每个层面相应的问题如下:
战略层面
8226; 缺乏战略规划,治疗领域过于宽泛,没有整合营销资源
职能层面
8226; 缺乏专门管理组织,凡事亲力亲为,要不临时抓个人顶,“爱谁谁”
操作层面
8226; 缺乏管理流程及相应制度,想到哪做到哪,“爱咋的咋的”
基于以上的分类,要解决新产品立项的问题就必须从这三层面加以管理。规范化操作是符合管理学要求的,但是战略层面的问题是宏观的,只能够规划,而职能和操作层面的问题是相对微观的,是可以规范化管理的。因此,要科学地解决新产品立项问题,首先必须制定研发战略,之后在战略实施阶段对职能和操作层面的问题加以规范化管理。很显然,新产品立项管理规范化主要体现在职能和操作层面,同时,也是研发战略实施的工具。
于是,老板们只要在制定研发战略的时候把好关,职能层面搭好班子,操作层面的具体工作就可以放手了。可是,忧心忡忡的老板们还是不放心:“立项的问题就落实了?谁来对这个事负责?有什么筛选标准?怎么个筛选法?”,这就引发了实现新产品立项管理规范化的三个方面,即立项管理的组织、立项筛选的流程和筛选的指标,那么新产品立项管理规范化也就是这三方面的相应规范化:建立专门立项组织、指标系统化和流程规范化。
建立专门立项组织
建立一个专门的机构负责立项管理,不能再由老板一个人拍脑瓜。但是很多企业在建立立项管理专门机构的时候都会犯一个错误:“新产品立项是研发的事,当然由研发的人负责。”可是研发人员往往精于专业技术而疏于营销知识,研发的产品多半和市场脱节,等到新产品上市阶段营销部门又抱怨:“这样的产品让我们怎么卖?”是的,按照整合营销的理论,研发是营销的起点,因此,作为研发起点的新产品立项应该不仅是研发的事,也是营销的事。因此,在建立立项管理机构(可称作新产品立项管理委员会,以下简称为立项委员会)的时候就应该加入营销部门的负责人,而不能是清一色的研发人员。当然,有一点要明确,立项委员会的负责人应该是主管研发的副总,毕竟新产品立项还是研发的工作量更多。营销副总作为市场专家身份加入委员会,以把握研发的市场导向性。同样,作为专家身份加入的还包括研究所(研发中心)的负责人,以及研发各职能部门的负责人。于是,新产品立项由老板一人拍脑瓜变为科研人员和营销人员集体智慧的结晶,孰优孰劣,地球人都知道!
新产品立项管理委员会组织结构图(图1)
指标系统化
指标系统化就是要解决拿什么来筛选新产品的问题,即建立评价新产品的指标体系,这套指标体系不但要客观地评价新产品的开发可行性,重要的是还要有可操作性。好比某人的择偶标准,有硬件要求:身高、年龄、学历;也有软件要求:长相、性格、修养等。硬件要求好办,一目了然,软件要求就麻烦了,本人不在就很难指操作了!指标系统化重点就是要解决如何将这些软件要求变得具有可操作性!
新产品立项评价指标的6个方面指标是:注册法规、知识产权、战略、市场因素、技术因素以及费用和周期,其中,注册法规、知识产权以及费用和周期属于刚性指标,因为这些指标分析得出的结果是“有或无”的概念,要么就是数字的量化概念;而战略、市场因素和技术因素是相对柔性的指标,因为这些指标很难用“有或无”或量化概念来评价。刚性指标是相对比较容易规范化管理的,因此新产品立项管理规范化关键是如何将这些柔性指标“刚性化”!
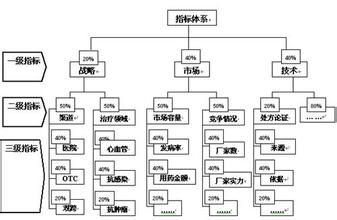
将柔性指标“刚性化”的过程其实就是将相对主观的指标客观化的过程。我们将主观指标客观化处理的常用方法是:先将主观指标尽可能分解细化(可采用分级的方法),再将这些细化后的指标按重要性分配权重,这样就行成一个评分系统,主观指标就被量化了。下面是战略、市场因素和技术因素三个柔性指标分解细化以及相应权重分配的示意图:
柔性指标分解细化以及相应权重分配的示意图(图2)
如上图所示,战略、市场和技术这样相对柔性的指标被逐级分解,分解到哪一级,应根据实际情况而定;每一级的指标都可按重要性的不同予以相应的权重。此外,在这些柔性指标当中也可以提炼出一些刚性的指标作为淘汰项,比如说市场容量小到某个定程度该项目就可以被淘汰,竞争厂家到多到一定数量也可以被淘汰。
于是,注册法规和知识产权两个刚性指标用于解决某个新产品是否能申报的问题;战略、市场因素和技术因素三个柔性指标经过 “刚性化”处理可以评价一个新产品的前景;费用和周期这个刚性指标可以给出新产品研发的投入成本。当这样包含众多市场和研发信息的指标分析结果摆到立项委员会的面前,相信大家最后做出的决策会比老板一个人拍脑袋强得多。在老板认可这些指标,或者他本人就亲自参与制定这些指标的前提下,老板对新产品的理念就固化到指标体系当中。
流程规范化
流程规范化是要建立一套新产品立项过程所需相应信息收集,分析的操作流程,以及各部门的权责和协作关系。首先,要确定评价指标体系各方面的指标分析调研的顺序,其次要明确每个指标由哪个部门负责分析调研;最后,要明晰各部门的工作交接和协作方式。
在新产品立项选筛过程中,为了避免出现重复性和不必要工作,提高工作效率,立项筛选按照以下先后顺序进行:法律和法规-知识产权-市场-技术-费用周期预算。每个部门在完成本部门的筛选工作后应通知下一个部门,并向新产品立项委员会负责人汇报;在紧急情况下,立项委员会可要求各部门同时进行筛选,筛选结果直接向立项委员会汇报,无需按先后顺序筛选、汇报结果。
新产品立项流程示意图(图3)
流程说明
1. 立项委员会在有新产品项目需筛选时,将项目的名称和需筛选内容(参见新产品筛选标准)作书面记录(研究中心完成)递交立项委员会负责人并抄送营销副总,由委员会负责人决定启动立项筛选,通知立项委员会所有成员。
2. 启动立项筛选后,研发中心负责人负责通知注册信息部门,进行注册法规及专利的查询。
3. 注册信息部门进行注册法规及专利的查询之后得出书面记录并汇报到立项委员会负责人,同时将筛选书面记录递交营销副总并通知(电话,电子邮件,传真)进行市场和战略调研。
4. 营销副总接到注册信息部门通知,安排市场部人员进行市场调研,完成市场调研并作书面记录向立项委员会负责人汇报,同时将筛选书面记录递交研发中心负责人并通知(电话,电子邮件,传真)进行技术调研。
5. 研发中心负责人接到市场部经理通知,安排研发人员进行技术调研,完成技术调研并
书面记录向立项委员负责人会汇报,同时安排研发人员进行费用周期预算。
6. 立项委员会负责人可依据汇报的筛选情况要求中止筛选、加快筛选(可要求各部门同时进行筛选)。(完)(任何发表、转载须先得到许可,联系方式:010-58671818-291/376)
 爱华网
爱华网